- 医学
新年号特集 免疫の謎を解き明かす
ヒト免疫の解明は医療に何をもたらすのか
対談・座談会 藤尾 圭志,西川 博嘉,金井 隆典,岡田 随象
2026.01.13 医学界新聞:第3581号より

自己免疫疾患,感染症,アレルギー,がん,神経難病……。免疫が何らかの形でかかわる疾患領域は膨大であり,免疫の異常そのものが病態の根幹をなしている疾患も少なくない。ヒト免疫の解明はこうした疾患群の根本的治療の実現に欠かせないだけでなく,再生医療や移植医療,がん治療やワクチン開発といった次世代医療の発展においても重要な意義を持つ。
医療の未来の鍵を握るヒト免疫研究の現在地点と展望を,トップランナーたちが語り合った。
藤尾 モデル動物を用いた研究により,免疫の基本的なメカニズムは20世紀までに概ね明らかになりました(「マウスとヒトの知見が交差する免疫学」・図2参照)。今は免疫介在性疾患の個別具体的な治療法を開発すべく,ヒトの免疫検体を用いた研究が加速している時代と言えるでしょう。本日は,消化器内科医として炎症性腸疾患(IBD)の免疫研究を牽引される金井先生,日本を代表するがん免疫の研究者であり,特に制御性T細胞(Treg)研究の臨床応用に尽力されている西川先生,そして大規模コンピューターを用いたゲノム解析で免疫疾患の解明や創薬をめざす遺伝統計学の分野をリードする岡田先生という,各領域のエキスパートにお集まりいただきました。ヒト免疫研究の現状や今後の展望について,広くお話しできればと思っています。よろしくお願いします。
科学の進歩でヒトの多様性・複雑性に挑む
金井 ヒト免疫の重要性を痛感したのは,IBDや関節リウマチ(RA)の特効薬として登場したTNF-α阻害薬がきっかけでした。実はマウスの研究ではあまり効果が出ていなかったにもかかわらず,ヒトでは劇的な成績を収めたのです。この時,「動物とヒトの免疫システムは違う」と思い知らされました。
西川 がん免疫の分野では同じ治療法でも効果に個人差が認められることが明らかになり,ヒトの複雑性,特にヒトという種の中での多様性を強く実感します。私がヒトのがん免疫研究に注力し始めた2000年代初頭は,まだまだヒトの複雑性・多様性へのアプローチが難しい状況がありました。しかし今はゲノムをはじめとするオミクス解析技術の発展により,こうした部分に正面からチャレンジできる時代になりました。その意味で,われわれの世代はラッキーであるとも感じています。
岡田 おっしゃるようにオミクス解析の発展は著しく,技術の高品質化,低価格化,スケールアップに伴い,ゲノムはもちろんですがシングルセル解析や空間トランスクリプトーム解析などが数多く実施されています。得られるデータ量が増え,既存の基礎医学研究や先生方が進められている臨床研究と結びつけて病態を分析できるようになり,私の専門とする遺伝情報学の観点からも非常に面白いフェーズに突入したと感じています。
藤尾 マルチオミクス解析技術の進歩の大きなポイントとして,ゲノムワイド関連解析(GWAS)では見えてこなかった,「なぜその遺伝子が疾患に関係するのか?」「免疫系のどこが病態と関係しているのか?」といった部分の解明に寄与している点が挙げられます。全身性自己免疫疾患の分野でも,私が構築に携わった大規模機能ゲノムデータベースImmuNexUT(図1)での解析情報などの大規模オミクスデータをもとに,RAや全身性エリテマトーデス(SLE)の病態や発症リスクの解明が大きく前進しました。
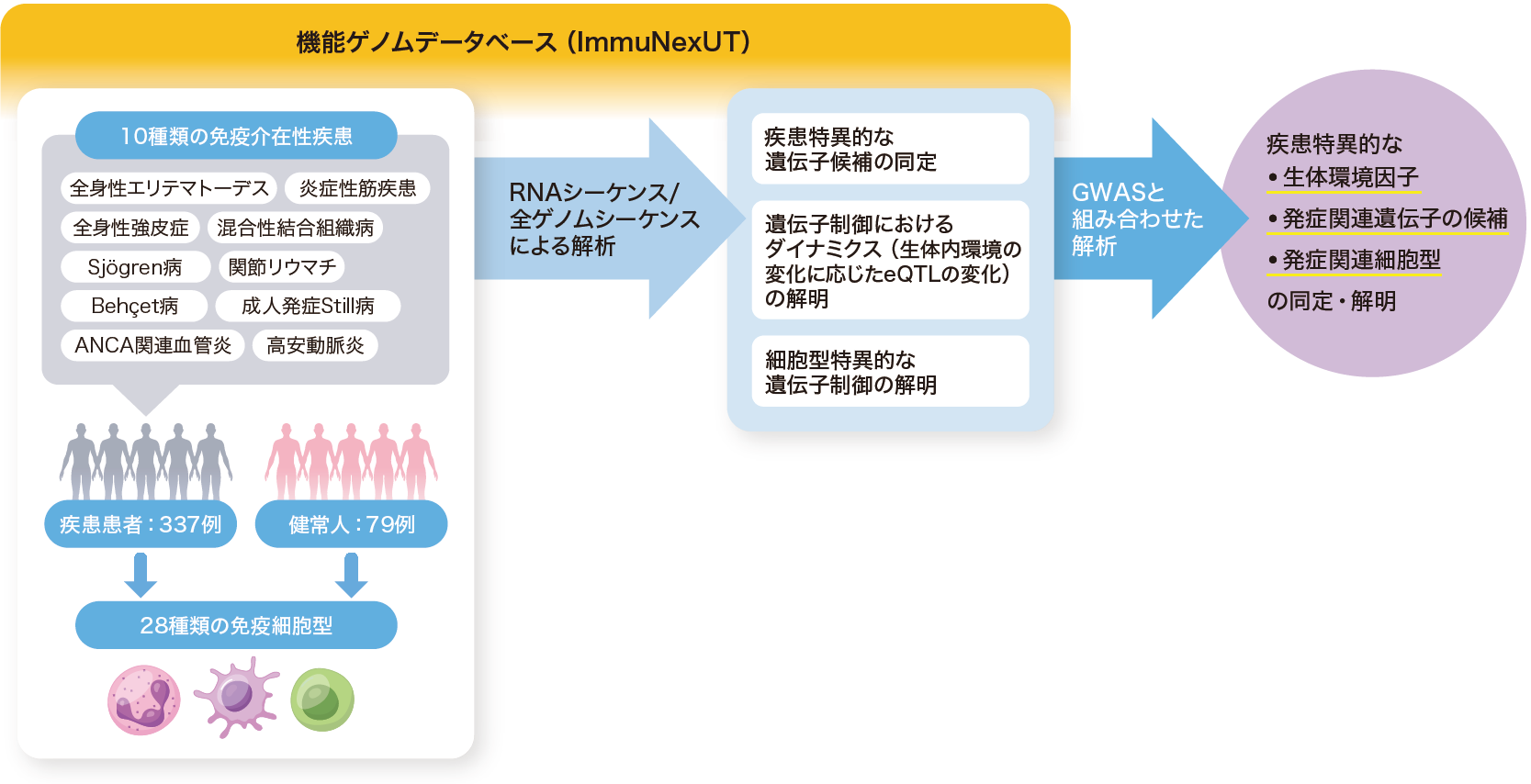
ある遺伝的特徴がどのように疾患の発症にかかわるかを解明するには,免疫細胞遺伝子発現データとゲノム情報に関する膨大なデータの解析が必要となる。国内では藤尾氏らが世界最大級の機能ゲノムデータベース(ImmuNexUT)を日本人患者のデータをもとに構築し,GWASとの組み合わせにより,免疫介在性疾患と関連する細胞や遺伝子を明らかにしている。
西川 研究スタイルもかつてはマウスからスタートし,得られた結果をヒトで検証していました。けれども今は治療効果が出ない患者群と治療が奏功している患者群の比較解析などから新しい分子を特定して,その重要性をマウスで確認し,ヒトへの応用につなげる「ヒトからマウスへ,マウスから再びヒトへ」という手法も可能な時代になっています。
藤尾 マウスとヒトの相互的な検証に加え,オミクス解析など基礎研究の知見がそのまま臨床に応用でき,臨床で得られたデータが再び基礎研究を加速させるという好循環は,免疫学ならではの魅力と言えるかもしれません(「マウスとヒトの知見が交差する免疫学」・図3参照)。
ヒト免疫研究の臨床応用に向けて
岡田 網羅的な俯瞰が可能になりつつある生体情報の中でも,血液はそのアクセスしやすさもあり,大量のデータを生み出す源泉となっています。組織としての血液は現段階でかなり詳細な理解が得られていると言っていいでしょう。一方で多くの免疫疾患は血液以外のアクセスしにくい臓器と連関しており,これらにおけるオミクス情報の統合はまだまだ不十分です。今後は血液以外の情報をいかに取得していくかが課題ですし,得られたデータを網羅的に分析して終わりとするのではなく,バイオマーカーを見つけ,特許を取得し,治療パッケージを作り,具体的な臨床利用につなげるという出口戦略までを考えていかなくてはなりません。
金井 自己免疫疾患は血液から病態の本質を読み取れるタイプと,そうでないタイプに大別されると思っています。私が専門とするIBDは後者に該当すると考えており,局所の組織採取を積極的に増やす必要性は身を持って感じています。
しかしながら大学病院という特性上,紹介をされてきた時点で既にステロイドなどの治療介入がなされている患者が一定数存在します。仮に検体が得られたとしても,研究対象に含めてよいのか迷う部分があることも事実です。例えばどの程度のステロイド投与量であれば研究対象に加えてよいのか,加えたとして果たしてその研究結果は真実を表しているのかといった点は,常に自問自答しています。IBDに対してもバイオ製剤や分子標的薬の活用が進んでおり臨床面での進歩を実感しますが,病態の解明という点では課題が多いですね。
藤尾 治療介入があった検体を研究上どう扱うかはおそらくどの領域も頭を悩ませるポイントでしょう。今後は日本全体で議論や仕組みづくりを進めていかねばなりませんね。
検体採取も含めヒト免疫において研究,臨床応用ともに進んでいるのはがん領域だと思いますが,このあたりの議論を踏まえて西川先生いかがでしょうか。
西川 免疫学での解析は,どれだけ分子発現の解析が進んだとしても機能解析こそが王道かつ最重要だと私は思っています。例えばある細胞に対してTregと思われるマーカーの発現が見られたとしても,最後は免疫抑制機能の解析がない限り,「この細胞はTregだ」とは言い切れません。そして機能解析のためにはやはり生きている細胞(検体)が必要になります。この点,がん研究領域は組織に直接アプローチできるので,他の疾患領域に比べると局所へのアクセスに関してアドバンテージがあると言えます。
以前は技術的な問題もあり,がん組織の微細な解析は難しいとされていました。しかし今ではがん細胞のゲノム情報をもとに,がんで免疫応答がどう調節されるかを明らかにする研究も進んでいます1,2)。また,ゲノム異常はがん細胞の増殖だけでなく免疫応答にも直接作用していることが明らかになってきており,がん細胞のゲノム解析と免疫解析を融合した研究が活発に進んでいます。
藤尾 臨床応用に関連して,薬物療法では免疫チェックポイント阻害薬や抗がん薬などさまざまな治療薬が選択肢になると思います。患者ごとの薬剤の有効性はどう予測しているのでしょうか。
西川 がん免疫療法(図2)の薬物療法では,PD-L1の発現や遺伝子変異量(TMB)といったバイオマーカーの検討に基づいて,最適な薬剤使用に向けた試みが実施されています。治療薬開発の発展とともに,近年は単剤での治療から併用療法が中心になってきました。ところが薬剤の併用により治療効果は向上したものの,逆に免疫関連有害事象(immune-related adverse events:irAE)の増加という新たな問題も生じています。そこで今後はバイオマーカーで患者を層別化し,より個別化するフェーズに移行しつつあります。
ここで難しいのがバイオマーカー研究です。論文化の際は統計的有意差が重要ですが,実際の臨床はそれだけでは十分ではありません。偽陽性・偽陰性をどれだけ減らせるかが重要で,理想は100%,少なくとも90%以上の精度がほしいかと思います。残念ながら,そこまでの結果はまだ出てきていないのが現状です。治療の順番や組み合わせの検討は進んでいる一方,「この治療はこの患者さんには効果が期待できないので,選択肢から外しても問題ない」との結論を出せるような段階には至っていません。
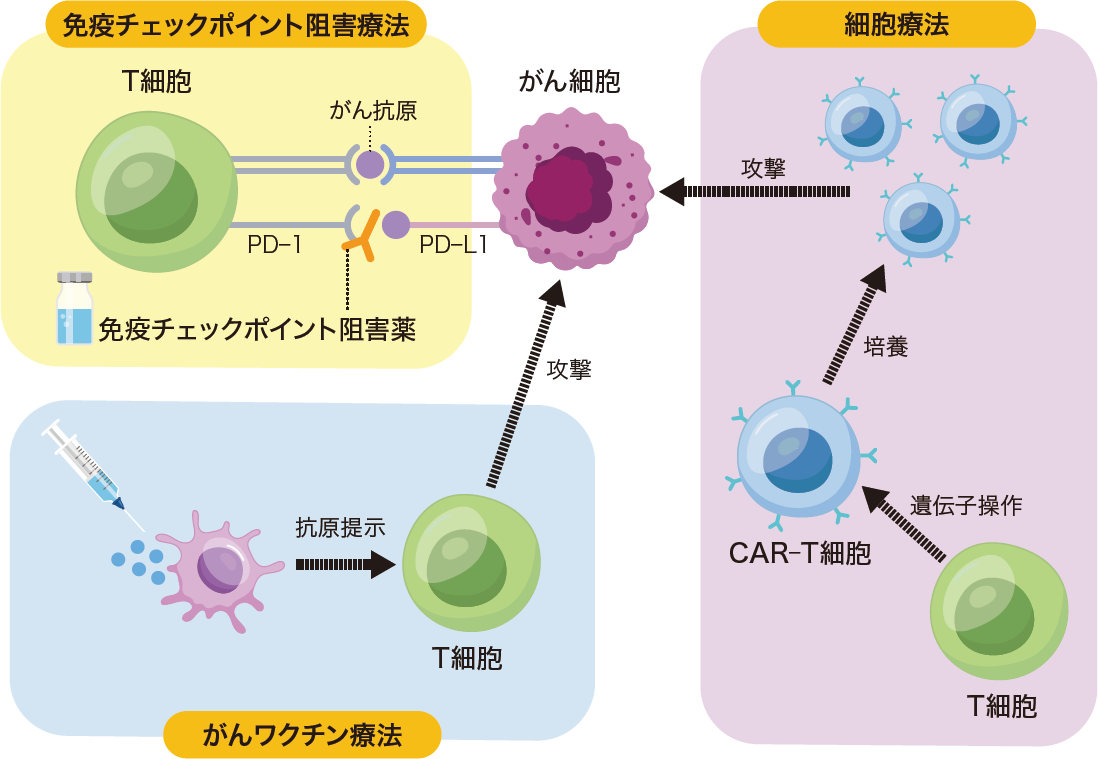
免疫チェックポイント阻害療法では,がん細胞による免疫のブレーキを解除し,再活性化したT細胞でがん細胞を攻撃する。細胞療法においては,患者自身のT細胞を遺伝子操作し培養したCAR-T細胞(キメラ抗原受容体遺伝子改変T細胞)によりがん細胞を攻撃する治療法が主に行われている。がんワクチン療法にはがん抗原を提示した樹状細胞の投与や,がん細胞の遺伝子情報に基づくがん抗原のmRNAワクチンなどがあるが,その多くは開発・臨床試験段階である。
AI・ビッグデータ時代に求められるwet・dryの二刀流
金井 基礎と臨床の距離が近いことがヒト免疫研究の魅力であることは事実です。しかし,いざ研究に注力するとき,実際は臨床と研究それぞれにかなりのエフォートを要しますので,この魅力はそのままハードルの高さにも直結します。私自身は内視鏡が導入された黎明期に医師になったこともあり,日中に内視鏡診療を行い,得られた検体の抽出・解析を夜通し行っていた時代もありました。けれども今の時代にそうした働き方,研究スタイルの励行はできません。ヒト検体を用いたwetの研究はどうしても時間的なコストがかかりますし,遺伝学的な解析やAI・データサイエンスの活用など,dryの研究手法もますます求められる時代になりました。こうした時代の変化を考慮すると,ヒト免疫の研究はかなりハードな道とも言える気がしています。
西川 研究を効率的に進めることは重要だと思います。私はアメリカの企業と協力し,組織検体を最大72時間安定して保存できる保存液や,組織検体を長期に凍結保存し,解凍後も生きたままの標本として細胞機能解析や組織の形態を維持したままで解析が可能な凍結液の開発を進めてきました。すでに商品化されており,こうした技術を駆使して効率的に研究を進め,研究者としてのQOL...
この記事はログインすると全文を読むことができます。
医学書院IDをお持ちでない方は医学書院IDを取得(無料)ください。

藤尾 圭志(ふじお・けいし)氏 東京大学大学院医学系研究科内科学専攻アレルギー・リウマチ学 教授
1995年東大医学部卒。2001年日本学術振興会特別研究員。02年東大大学院医学系研究科内科学専攻博士課程修了。06年東大病院アレルギー・リウマチ内科助教,17年より同科科長および現職。臨床に従事する傍ら自己免疫疾患を中心としたヒト免疫の研究に尽力し,21年には東大病院アレルギー・リウマチ内科の患者データを基に構築した世界最大規模の機能ゲノムデータベース「ImmuNexUT(Immune cell gene expression atlas from the University of Tokyo)」の構築に携わる。

西川 博嘉(にしかわ・ひろよし)氏 国立がん研究センター腫瘍免疫研究分野 分野長
1995年三重大医学部卒。2002年同大大学院医学研究科内科学専攻博士課程修了。03年メモリアル・スローン・ケタリングがんセンターリサーチフェロー,06年三重大大学院医学系研究科病態解明医学講座講師,10年阪大免疫学フロンティア研究センター実験免疫学特任准教授を経て,15年より現職。16年より名大大学院医学系研究科微生物・免疫学講座教授をクロスアポイントメント。24年からは京大大学院医学研究科附属がん免疫総合研究センター がん免疫多細胞システム制御部門教授も兼任する。

金井 隆典(かない・たかのり)氏 慶應義塾大学医学部内科学教室消化器内科 教授
1988年慶大医学部卒。94年同大大学院医学研究科博士課程修了。95年米ハーバード大学ベス・イスラエル医療センターリサーチフェロー,2000年東京医歯大(当時)病院第一内科学助手を経て,08年より慶大医学部消化器内科准教授。13年より現職。同年から慶大免疫統括医療センターセンター長,同大病院IBDセンター センター長などを兼任する。20年にはCOVID-19パンデミックの中で,コロナ制圧タスクフォースの研究統括責任者を務めた。

岡田 随象(おかだ・ゆきのり)氏 東京大学大学院医学系研究科遺伝情報学 教授
2005年東大医学部卒。臨床研修を修了後,基礎研究者になることを決意し同大大学院医学研究科内科学専攻へ進学し,11年に博士課程修了。大学院ではヒトゲノムデータの解析手法を学ぶ。日本学術振興会特別研究員(DC2,PD),米ハーバード大ブリガム・アンド・ウィメンズ病院ブロード研究所研究員などを経て,16年より阪大大学院医学系研究科遺伝統計学教授。21年より理化学研究所生命医科学研究センターチームディレクターを併任。22年より現職。
いま話題の記事
-
ピットフォールにハマらないER診療の勘どころ
[第22回] 高カリウム血症を制するための4つのMission連載 2024.03.11
-
VExUS:輸液耐性が注目される今だからこそ一歩先のPOCUSを
寄稿 2025.05.13
-
寄稿 2025.11.11
-
医学界新聞プラス
[第1回]★1を見た夜――評価社会を生きる医療者のために
★1の向こう側連載 2026.05.18
-
サルコペニアの予防・早期介入をめざして
AWGS2025が示す新基準と現場での実践アプローチ寄稿 2026.03.10
最新の記事
-
対談・座談会 2026.05.12
-
生涯を通じて女性のQOLを維持・向上する
産婦人科4本目の柱「女性医学」対談・座談会 2026.05.12
-
Sweet Memories
揺れながら進む,あなたの一歩に意味がある寄稿 2026.05.12
-
デジタル撮像とAIが切り拓く,細胞診の新たな地平
新田 尚氏(株式会社CYBO 代表取締役社長)に聞くインタビュー 2026.05.12
-
そのとき,研修医と指導医は何を考えているのか
麻酔科における「時間の流れ」と「思考の進め方」寄稿 2026.05.12
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。