RCTと観察研究――デザインの違いと意味するものの違い 2(植田真一郎)
連載
2009.07.06
論文解釈のピットフォール
【第4回】
RCTと観察研究――デザインの違いと意味するものの違い 2
植田真一郎(琉球大学大学院教授・臨床薬理学)
(前回からつづく)
ランダム化臨床試験は,本来内的妥当性の高い結果を提供できるはずですが,実に多くのバイアスや交絡因子が適切に処理されていない,あるいは確信犯的に除 去されないままです。したがって解釈に際しては,“ 騙されないように” 読む必要があります。本連載では,治療介入に関する臨床研究の論文を「読み解き,使う」上での重要なポイントを解説します。
なぜRCTと観察研究の結果が異なるのか?
前回は観察研究の限界について述べました。例として挙げた閉経後女性のホルモン補充療法(Hormone Replacement Therapy:HRT)では,観察研究では心筋梗塞のリスクを下げるという結果が出たのに,ランダム化臨床試験(RCT)ではむしろリスクを増すという結果になっています。この違いはどこから生じたのでしょうか? 今回は,ランダム化されていないことの弱点から考えてみましょう。
まず考えつくのは社会的な背景の違いです。実際,コホート研究でHRTを受けていた女性は高卒以上の学歴を持つものが多い,白人が多い,既婚者が多いなどの報告があり,これらは健康に関する意識の違いなどで心筋梗塞リスクに影響する可能性がありますね。社会経済的な背景の補正を行うと,結果はよりRCTに近づくという報告もあります。
また,HRTを受けている女性はほかの薬剤に関してもその意味を理解し,きちんと服用する,すなわちアドヒアランス(以前はコンプライアンスといいました)が良い可能性があります。興味深いことに,これまでのいくつかの冠動脈疾患臨床試験では,プラセボ群でもアドヒアランスの良い患者さんの予後が良いことが報告されているのです。つまり,コホート研究でのHRT群は「アドヒアランス良好群」とも言えるわけですね。すなわち暴露因子HRTが心筋梗塞リスク減少の原因ではなく,交絡因子として「アドヒアランス良好」があり,こちらが結果に影響したのかもしれません。観察研究でこの点を克服するには,ある程度教育レベルの均一な集団を対象にするなどの方法があると思います。ただし看護師を対象に行われた研究(Nurses' Health Study)では,社会経済的背景の違い,アドヒアランスの違いは大きくなかった可能性はありますが,RCTとは異なる結果が出ています(文献1)。
次に「医師の裁量」はどうなるでしょうか。考えられるのは,より心血管リスクの低い女性に投与している可能性です。実際,HRTを受けている女性は受けていない女性と比較して血圧,血中インスリン値が低い,体重が少ない,身体活動性が高いなどとする報告もあります。これは先述した「健康への意識の違い」のほかに,経口避妊薬の血栓症,心筋梗塞リスク上昇の可能性から,医師がハイリスクの女性を避けた可能性もあるのではないでしょうか。このあたりの交絡因子の除去や選択バイアスの回避にはやはりランダム化割り付けが有効で,これまでに述べた因子は各群同等に分布することが予想されます。
次にアウトカムの評価から考えてみましょう。前述したNurses' Health Studyでは,2年ごとのアンケート調査や本人,家族からの報告などでイベントを評価しています。しかし,診療録へのアクセスは常に可能というわけではないでしょうし,死亡した場合も遺族を介してのイベント評価となるので,精度がRCTよりも劣ると考えられます。RCTではもちろん担当医から直接報告されますし,診療録の閲覧もより容易だと思います。
また,Nurses' Health Studyでは症状のない,あるいは症状が典型的ではない心筋梗塞は除外されています。つまり,このようなコホート研究における心筋梗塞,冠動脈疾患死の評価の難しさが結果に影響した可能性があると思います。欧米のRCTはそれが市販後であっても治験と同じ規則GCP(Good Clinical Practice)を遵守することが求められます。日本の厚労省省令GCPとは若干異なりますが,あの煩雑な治験と同じように患者を登録し,データを収集し,アウトカムを評価することを想像してみてください。アウトカムによってはコホート研究とは精度がまったく違うということになってしまいますね。
RCTの弱点とは?
At its best, a trial shows what can be accomplished with a medicine under careful observation and certain restricted conditions. The same results will not invariably or necessarily be observed when the medicine passes into general use
(Austin Bradford Hill, 1984)
これまで,RCTの強みについて述べてきました。それはランダム化であり,より厳密な評価であるわけですが,弱点ももちろんあります。例えば,そのような強みを持つが故に特殊な環境下で行われるいわば「実験」となり,結果を通常の診療で用いることが容易ではないということです。このパラグラフの冒頭のHill氏のことばがそれを端的に表しています。Hill氏は世界初のRCTであるストレプトマイシン研究をデザインした統計学者ですが,その限界もよく認識していました。
本来,臨床試験をデザインするときには,広く結果を適用できるようにすべきですが,多くの努力は結果の信頼性(内的妥当性)を高めるためと安全性を確保するために費やされます。これは,RCTが本来新薬の効能(efficacy)を安全にかつ厳密に評価する,という使命を負っているからにほかなりません。治験の研究計画書をみるとうんざりするくらい(うんざりしてはいけませんが)選択基準,除外基準が列記されていますね。そしてその治験をしようと思っても,結局受け持ち患者さんのうち登録できる人はごく少ないことに気付きます。そうすると,その治験(もちろん治験も臨床試験の一つであり,多くは二重盲検法を用いたRCTです)の結果が適用できる患者もごく少ない,ということになってしまいます。
しかし先述したように,安全性を確保しつつ効能を厳密に評価するためには仕方のないことでもあります。したがって,まったくの新薬ではなくても,長期的な予後を評価する臨床試験を行う場合,特に対象疾患がこれまでと異なる場合,同様なデザイン,すなわち厳しい患者選択除外基準,細部まで定められた治療プロトコル,二重盲検法などが用いられています。これらがRCTの強みであり,弱みにもなるのです。安全性に関して,そのようなRCTの結果が必ずしも現実には通用しないことがあります。
臨床試験では安全でも……
スピロノラクトンという抗アルドステロン薬とプラセボを,重症心不全を対象に予後を比較したRALES研究という臨床試験があります(文献2)。その結果,スピロノラクトン群での生存率が良いことが報告され,抗アルドステロン薬は重症心不全の薬剤として認められました。この研究後,スピロノラクトンの処方は増え,RALES研究の前に比較すると3倍になりました(図1,文献3)。
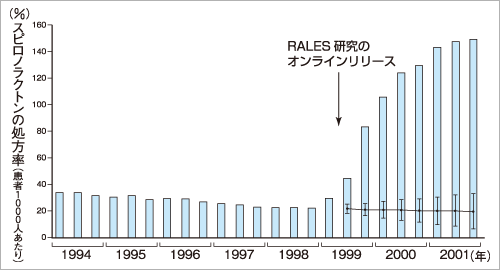 |
| 図1 入院したACE阻害薬服用中の心不全患者におけるスピロノラクトンの処方率 |
| RALES研究の発表後,スピクロノラクトンの処方率は3倍になっていることがわかります。 |
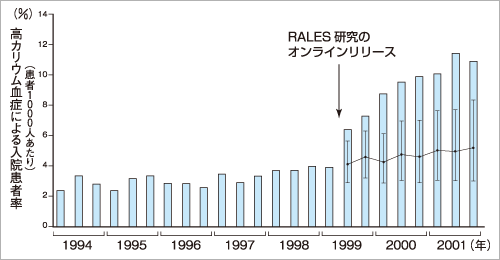
ところが,なんと高カリウム血症による死亡も倍増したのです(図2)。もちろんカリウム保持性利尿薬を心不全標準薬であるACE阻害薬と併用するわけですからその危険性は予測できたわけですが,RALES試験でのカリウム上昇はわずか0.3mmol/Lに過ぎず,クレアチニン上昇も0.05-0.1mg/dL,重篤な高カリウム血症の発生は1.7%でした。プラセボ群でも1.2%あったので,絶対リスクの増加はわずか0.5%だったのです。
 |
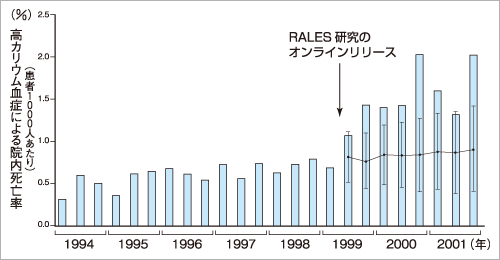 |
| 図2 (上)ACE阻害薬を服用している心不全患者における,高カリウム血症による入院患者の割合,(下)および高カリウム血症による入院中死亡率 |
| RALES研究の発表後,これらの割合が明らかに増加していることがわかります。 |
では,なぜ実際の診療では高カリウム血症が増加したのでしょうか? まず,RALES研究の患者の平均年齢は65歳であり,合併症が多く,腎機能も低下している高齢者があまり含まれていません。現実の診療を反映する心不全のコホート(文献3)では平均年齢は75歳を超え,腎機能も低下していることが予想されるので,高カリウム血症のリスクは高くなりますね。心不全に限らず多くの動脈硬化性疾患臨床試験では,やはり高齢者や女性,合併症を有する患者さんの割合が実際の診療とは異なることが多いようです。また,RALES試験ではループ利尿薬の使用が100%であることも影響した可能性があります。
このようなリスクの高い患者への新薬(あるいは新たな対象疾患)の臨床試験では,安全性を確保するためにランダム化の前に,Placebo run-in periodを設けて薬剤の安全性を個々にチェックすることがあります。例えば,同じく心不全患者におけるβ遮断薬カルベジロールの臨床試験では,低用量のカルベジロールをこの期間に投与し,有害事象が発生するようであれば試験から除外しました(文献4)。これは全体の5.6%にもなりましたから,もしこの患者たちが試験に入っていたとすると,結果に影響するはずです。スピロノラクトンにしても,カルベジロールにしても,その疾患に関しては初めての臨床試験であったので,安全性への配慮は倫理的にも必須であり,このようなプロトコルは必要であったのです。また,医師が初めてカルベジロールを使用するときにこういった方法は参考になると思います。したがって,安全性を確保するためのプロトコル,選択除外基準はこの段階の試験では必要で,外的妥当性よりも重視すべきなのです。しかし,この結果を安全性も含めて多くの患者さんへ適用するには,別の研究が必要になります。次回はそのあたりを解説します。
(つづく)
参考文献
1)Stampfer MJ, et al. Postmenopausal estrogen therapy and cardiovascular disease.Ten‐year follow‐up from the nurses' health study. N Engl J Med 1991;325(11):756-62.
2)Pitt B, et al. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. N Engl J Med 1999; 341(10):709-17.
3)Juurlink DN, et al. Rates of hyperkalemia after publication of the Randomized Aldactone Evaluation Study. N Engl J Med. 2004;351(6):543-51.
4)Packer M, et al. The effect of carvedilol on morbidity and mortality in patients with chronic heart failure. U.S. Carvedilol Heart Failure Study Group. N Engl J Med. 1996;334(21):1349-55.
いま話題の記事
-
忙しい研修医のためのAIツールを活用したタイパ・コスパ重視の文献検索・管理法
寄稿 2023.09.11
-
人工呼吸器の使いかた(2) 初期設定と人工呼吸器モード(大野博司)
連載 2010.11.08
-
連載 2010.09.06
-
事例で学ぶくすりの落とし穴
[第7回] 薬物血中濃度モニタリングのタイミング連載 2021.01.25
-
寄稿 2016.03.07
最新の記事
-
医学界新聞プラス
[第3回]わかりやすく2つの軸で分類して考えてみましょう
『心理社会的プログラムガイドブック』より連載 2024.04.26
-
医学界新聞プラス
[第1回]平坦な病変 (1)色調の変化があるもの
『内視鏡所見のよみ方と鑑別診断——上部消化管 第3版』より連載 2024.04.26
-
医学界新聞プラス
[第1回]心エコーレポートの見方をざっくり教えてください
『循環器病棟の業務が全然わからないので、うし先生に聞いてみた。』より連載 2024.04.26
-
医学界新聞プラス
[第1回]バルーン閉塞下逆行性経静脈的塞栓術(BRTO)
『IVRマニュアル 第3版』より2024.04.26
-
医学界新聞プラス
[第4回]脆弱性骨盤骨折
『クリニカル・クエスチョンで考える外傷整形外科ケーススタディ』より連載 2024.04.26
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。
