- HOME
- 医学界新聞プラス
- 医学界新聞プラス記事一覧
- 2024年
- 医学界新聞プラス [第4回]疾患編:慢性虚血性心疾患――虚血と心筋バイアビリティの評価 虚血評価評価の意義,予後予測におけるMRI
医学界新聞プラス
[第4回]疾患編:慢性虚血性心疾患――虚血と心筋バイアビリティの評価 虚血評価評価の意義,予後予測におけるMRI
『心臓疾患のCTとMRI 第2版』より
連載 髙藤雅史,石田正樹
2024.12.06
心臓疾患のCTとMRI 第2版
前版となる『心臓血管疾患のMDCTとMRI』が2005年に刊行されてから19年が経過した2024年,待望の第2版となる『心臓疾患のCTとMRI』がこのたび刊行されました。この間,心臓CTやMRIの有効性に関するエビデンスの蓄積が進んだことから,さまざまな心疾患のガイドラインにおいて心臓CTやMRIの存在感が高まっており,検査に必要な解剖と撮影断面,撮影法の基礎と実践,画像解析と表示法,画像診断の適応となる疾患の基礎と読影のポイントを紹介した本書は,日々の臨床に役立つこと間違いなしです。医学界新聞プラスでは,本書の中から4項目をピックアップし,ご紹介していきます。ぜひご覧ください。
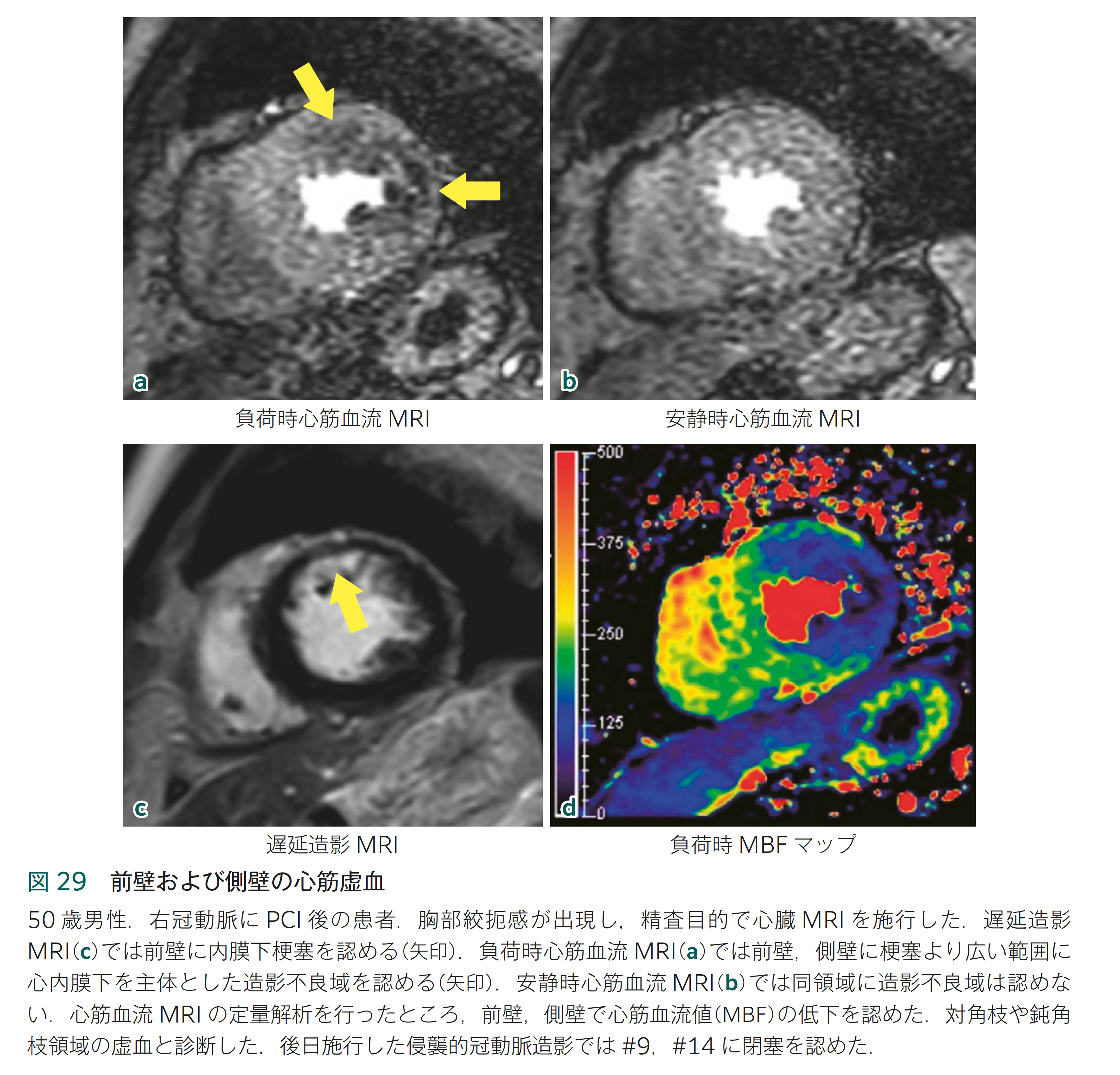
●負荷心筋パーフュージョンMRIによる虚血評価(図29)
負荷心筋パーフュージョンMRIは,安静時およびATPなどによる薬剤負荷中にガドリニウム造影剤をボーラス静注して左室心筋をダイナミック撮影し,心筋ファーストパス時の心筋造影効果の局所的な低下(perfusion defect)を検出し心筋虚血を診断する検査法である.
負荷心筋パーフュージョンMRIの読影法
負荷心筋パーフュージョンMRIの読影は,通常,視覚評価で行う.負荷時,安静時の心筋パーフュージョンMRIとこれらと同一断面の遅延造影MRIを並べて表示し比較しながら読影する.最初に,薬剤負荷が適切であったか確認する.検査時のバイタルサインの記録を参照し,薬剤負荷に対して,心拍数が安静時より10bpm以上増加したか,収縮期血圧が10mmHg以上低下したかを確認する.また,脾臓の最大増強効果が負荷時に低下するsplenic switch offという現象がみられているかを確認する1).これらが確認できない場合,薬物負荷が十分でなかった可能性があり,虚血の所見が認められなくても偽陰性の可能性がある.負荷心筋パーフュージョンMRIでは,表在冠動脈狭窄による心筋虚血は,心筋ファーストパスにおける当該動脈の灌流領域の内膜下優位の造影効果の低下(perfusion defect)として診断される.典型的には心筋虚血を示す負荷時心筋のperfusion defectは左室内腔血液信号のピークから3~5心拍続き,心内膜下で最も顕著であり,しばしば心外膜側へ向かって徐々に弱くなる勾配を示す.遅延造影MRIで梗塞がみられる場合は,梗塞のない心筋領域で上記のとおり判定する.心筋パーフュージョンMRIは空間分解能が高く冠動脈多枝病変の評価にも優れる.三枝病変では典型的には,全周性に心内膜下優位の負荷時perfusion defectを示すが,表在冠動脈一枝領域あるいは二枝領域の血流異常が顕著になる場合があり診断に苦慮することがある.また,表在冠動脈に狭窄のない微小循環障害の場合も,三枝病変と同様に全周性に心内膜下血流低下を認めることがあり三枝病変との鑑別が難しい2).近年,心筋血流MRIの定量解析(図29)が普及してきており,三枝病変や微小循環障害の診断,鑑別に有用である可能性が示されている3).
負荷心筋パーフュージョンMRIの診断能
負荷心筋血流MRIによる冠動脈疾患の診断能については多数の報告がある.冠動脈造影による形態的な狭窄度をリファレンスとした場合の診断能は,メタ解析によると,50%以上の冠動脈狭窄の検出に対する感度・特異度は,それぞれ,1.5T装置で82%,75%,3.0T装置で90%,79%であり,70%以上の冠動脈狭窄の検出に対する感度・特異度は,それぞれ,1.5T装置で86%,77%,3.0T装置で91%,74%である4).冠血流予備量比(FFR)による冠動脈の機能的狭窄を基準とした場合の診断能は,メタ解析によると,感度,特異度はそれぞれ,89%,87%,AUCは0.94である5).Ishidaら6) は,侵襲的冠動脈造影における70%以上の冠動脈狭窄に対する負荷心筋血流MRIとSPECTの診断能を比較し,心筋血流MRIはSPECTと比べ有意に診断能が優れていることを示した(AUC=0.89~0.91 vs. 0.71~0.75, p<0.05).また,単施設ランダム化研究であるCE-MARC studyでも,冠動脈造影で50%以上の冠動脈狭窄をリファレンスとした場合,心筋パーフュージョンMRIはSPECTと比べ有意に診断能が優れていた(AUC=0.89 vs. 0.74, p<0.0001)7).同様にメタ解析でも,負荷心筋血流MRIはSPECTと比べ診断能が優れていることが示されている(AUC=0.97 vs. 0.74)8).
負荷心筋パーフュージョンMRIのガイドラインにおける位置づけ
日本循環器学会の「安定冠動脈疾患の血行再建ガイドライン(2018年改訂版)」では冠動脈疾患の中等度リスクを有する症例に対して,負荷心筋パーフュージョンMRIを含む負荷イメージングを用いた虚血評価を行うことが推奨されている(推奨クラスⅠ,エビデンスレベルA)9).ヨーロッパ循環器学会の「慢性冠症候群の診断と治療のガイドライン(2019年)」では,冠動脈疾患を臨床評価のみで除外できない有症状患者において,負荷心筋パーフュージョンMRIなどによる心筋虚血評価は冠動脈疾患診断の初期検査として推奨されている(推奨クラスⅠ,エビデンスレベルB)10).アメリカ心臓病学会/アメリカ心臓協会の「胸痛ガイドライン(2021年)」では,急性冠症候群が除外された急性胸痛あるいは,安定胸痛いずれのシナリオにおいても,既知の冠動脈疾患がなく,冠動脈疾患の中等度以上のリスクを有する患者に負荷心筋パーフュージョンMRIを含む負荷イメージングを実施することが強く推奨されている(推奨クラスⅠ,エビデンスレベルB-NR)11).同ガイドラインでは,有意狭窄のない冠動脈があり安定胸痛が持続するINOCA(Ischemia and No Obstructive Coronary Artery)が疑われる患者に対して,定量的負荷心筋パーフュージョンMRIにより心筋血流予備能を評価することは,微小血管機能障害の診断とリスク層別化に有効であるとされる(推奨クラスⅡa,エビデンスレベルB)11).一方,米国の多施設レジストリ研究(SPINS)の2,349名の後向き解析では,心筋血流MRIで虚血を認めた患者は認めない患者に比べ3倍以上心血管イベントが多く,虚血を認めるセグメントが多いほど心血管イベントが増加したことが示されており,虚血性心疾患患者の心筋虚血の重症度の評価において負荷心筋パーフュージョンMRIが有用であることが示されている12).これらを反映して,日本循環器学会の「安定冠動脈疾患の診断と治療のガイドライン フォーカスアップデート版(2022年)」では,冠動脈疾患の検査前確率・臨床的尤度に基づいた適切な検査選択を行い,中等度以上の事前確率を有する患者に対しては,負荷心筋パーフュージョンMRIを含む負荷イメージングを実施し患者リスク評価を行うことが推奨されている13).
●遅延造影MRIによる心筋バイアビリティ評価(図30)
遅延造影MRIはガドリニウム造影剤投与後10分程度経過して撮影され,正常心筋の信号値をゼロにすることで心筋梗塞や線維化を高信号領域として描出する方法である.高い空間分解能およびコントラストにより心筋梗塞領域を正確に診断することができ,非侵襲的な梗塞診断のゴールドスタンダードとされる.
遅延造影MRIの読影法
遅延造影MRIは,同一断面のシネMRI画像と並べて表示し,比較しながら読影する.遅延造影MRIでは心筋梗塞は,心内膜下を主体とし冠動脈支配に一致した高信号域として認められる(図30).複数の断面で遅延造影の領域を確認することで心筋梗塞の部位と広がりを正確に診断することができる.梗塞の壁内深達度,生存心筋壁厚の評価は,部分容積現象による過大評価を避けるため,必ず梗塞心筋の直交断面で行う.急性心筋梗塞例における梗塞範囲の評価は,基本的には陳旧性梗塞の評価と同様であるが,no-reflowを示す心内膜下および心筋中層の低信号域(microvascular obstruction;MVO)がみられた場合は,これを梗塞領域に含めて評価する.正常心筋の無信号化(nulling)が不良の場合,梗塞心筋と生存心筋のコントラストが不良となり,梗塞の広がりを正しく評価できなくなるため,遅延造影MRIの撮影においては正しいnullingによる撮影が最も重要である.null pointの設定を厳密に行わなくても正常心筋が黒く描出されるPSIR法の併用も有用である.また,心電図同期不良や息止め不良,撮影断面内に脳脊髄液,胸水,胃内容物などのT1値の長い構造がある場合などでは,高信号のゴーストアーチファクトを呈することがある14).このようなアーチファクトが疑われた場合は,位相方向を変えた撮影や多断面での撮影を確認することでアーチファクトと梗塞を鑑別できる場合がある.そのため撮影時にこれらの追加撮影を適切に行うことが重要である.
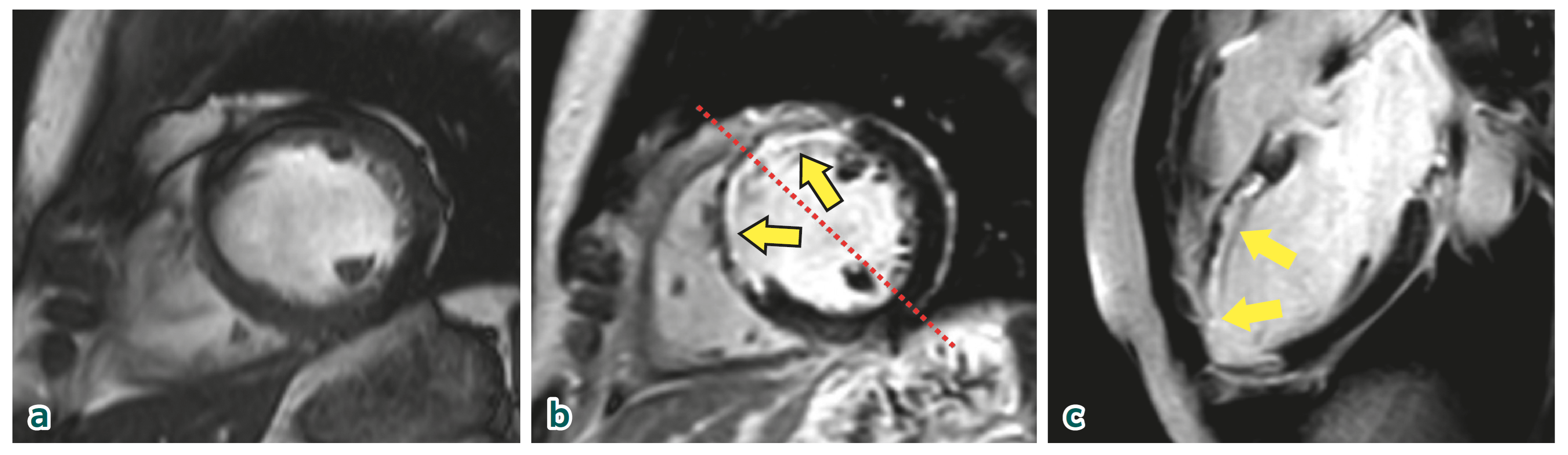
60歳代男性.6年前に急性心筋梗塞にて左冠動脈前下行枝にPCIを施行された患者.シネMRIの短軸像(a),遅延造影MRIの短軸像(b)と前壁中隔の梗塞(矢印)に対する直交断面(c)を示す.壁内深達度は75%以上で心尖部では100%である.バイアビリティは乏しいと診断した.
遅延造影MRIによる心筋バイアビリティ診断
遅延造影MRIでみられる心筋梗塞の壁内深達度は,再灌流療法後の左室機能回復と逆相関の関係にあり,心筋バイアビリティ評価に用いられる.再灌流治療前に左室機能異常がみられた慢性冠動脈疾患患者50名を対象に遅延造影MRIの梗塞の壁内深達度と再灌流治療後の左室の局所機能回復との関連をみた検討によると,梗塞の壁内深達度が50%を超えると機能回復はほとんどみられない(7.7%,14/182)のに対して,50%未満では66.1%(411/622)の症例で左室壁運動の改善がみられたと報告された15).また,急性心筋梗塞患者における報告では遅延造影MRIでの梗塞の壁内深達度50%をカットオフとした場合,92.0%の正診率で局所の機能回復を予測できることが示されている16).一方,心筋梗塞や左室容積の拡張により菲薄化した心筋においては,梗塞の壁内深達度からバイアビリティ評価を行うことは難しい場合が多い.このような場合には生存心筋の壁厚がバイアビリティ評価に役立つ.心筋梗塞後,生存心筋の壁厚が,急性期に3.9mm以上,慢性期に5.1mm以上である場合,それぞれ79.6%,88.4%の正診率で機能回復を予測できる17).
遅延造影MRIのガイドラインにおける位置づけ
遅延造影MRIによる再灌流療法前の心筋バイアビリティ評価の有用性については,単施設研究によるエビデンスが中心である.本項執筆時点では,ヨーロッパ循環器学会の「再灌流療法に関するガイドライン(2018年版)」において,冠動脈疾患と駆出率低下型心不全を有する患者において再灌流療法を行う前に遅延造影MRIで心筋バイアビリティ評価を行うことは,推奨クラスⅡb,エビデンスレベルB18),日本循環器学会の「慢性冠動脈疾患診断ガイドライン(2018年改訂版)」においては,冠動脈疾患を有し,冠動脈血行再建術が適応と考えられる心不全症例に対して血行再建術前に遅延造影MRIを施行することは,推奨クラスⅡa,エビデンスレベルBにとどまる9).一方,遅延造影MRIにおける梗塞診断は冠動脈疾患患者の予後予測において有用である.海外の報告では遅延造影MRIで6セグメント以上の領域に心筋梗塞を認めた冠動脈疾患患者は6セグメント以下の患者に比べ,有意に心血管イベントが多かったことが示された19).また前述のSPINSレジストリにおいても,心筋血流MRIにおける虚血と,遅延造影MRIにおける梗塞の両方を認めた患者は,認めなかった患者に比べ,年間心血管イベント発症率が4倍以上,心臓MRI後1年間の再灌流療法が施行される割合が10倍以上高かったことが示されている12).
文献
1)Manisty C, et al:Splenic Switch-off:A Tool to Assess Stress Adequacy in Adenosine Perfusion Cardiac MR Imaging. Radiology 276:732-740, 2015
2)Panting JR, et al:Abnormal subendocardial perfusion in cardiac syndrome X detected by cardiovascular magnetic resonance imaging. N Engl J Med 346:1948-1953, 2002
3)Kotecha T, et al;Assessment of Multivessel Coronary Artery Disease Using Cardiovascular Magnetic Resonance Pixelwise Quantitative Perfusion Mapping. JACC Cardiovascular imaging 13:2546-2557, 2020
4)Kiaos A, et al:Diagnostic performance of stress perfusion cardiac magnetic resonance for the detection of coronary artery disease:A systematic review and meta-analysis. Int J Cardiol 252:229-233, 2018
5)Takx RA, et al:Diagnostic accuracy of stress myocardial perfusion imaging compared to invasive coronary angiography with fractional flow reserve meta-analysis. Circulation Cardiovascular imaging 8:e002666, 2015
6)Ishida N, et al:Noninfarcted myocardium:correlation between dynamic first-pass contrast-enhanced myocardial MR imaging and quantitative coronary angiography. Radiology 229:209-216, 2003
7)Greenwood JP, et al:Cardiovascular magnetic resonance and single-photon emission computed tomography for diagnosis of coronary heart disease(CE-MARC):a prospective trial. Lancet 379:453-460, 2012
8)Danad I, et al:Diagnostic performance of cardiac imaging methods to diagnose ischaemia-causing coronary artery disease when directly compared with fractional flow reserve as a reference standard:a meta-analysis. Eur Heart J 38:991-998, 2017
9)Yamagishi M, et al:JCS 2018 Guideline on Diagnosis of Chronic Coronary Heart Diseases. Circ J 85:402-572, 2021
10)Knuuti J, et al:2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J 41:407-477, 2020
11)Gulati M, et al:2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR guideline for the evaluation and diagnosis of chest pain:a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol 78:e187-e285, 2021
12)Kwong RY, et al:Cardiac Magnetic Resonance Stress Perfusion Imaging for Evaluation of Patients With Chest Pain. J Am Coll Cardiol 74:1741-1755, 2019
13)Nakano S, et al:JCS 2022 guideline focused update on diagnosis and treatment in patients with stable coronary artery disease. Circ J 86:882-915, 2022
14)Saremi F, et al:Optimizing cardiac MR imaging:practical remedies for artifacts. Radiographics 28:1161-1187, 2008
15)Kim RJ, et al:The use of contrast-enhanced magnetic resonance imaging to identify reversible myocardial dysfunction. N Engl J Med 343:1445-1453, 2000
16)Kitagawa K, et al:Acute myocardial infarction:myocardial viability assessment in patients early thereafter comparison of contrast-enhanced MR imaging with resting(201)Tl SPECT. Single photon emission computed tomography. Radiology 226:138-144, 2003
17)Ichikawa Y, et al:Late gadolinium-enhanced magnetic resonance imaging in acute and chronic myocardial infarction:Improved prediction of regional myocardial contraction in the chronic state by measuring thickness of nonenhanced myocardium. J Am Coll Cardiol 45:901-909, 2005
18)Neumann FJ, et al:2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J 40:87-165, 2019
19)Kelle S, et al:Prognostic value of myocardial infarct size and contractile reserve using magnetic resonance imaging. J Am Coll Cardiol 54:1770-1777, 2009
心臓疾患のCTとMRI 第2版
心臓疾患の画像診断の決定版となるテキスト
<内容紹介>画像解剖から、CT・MRIの撮影法、各疾患への適応とプロトコール、診断までを網羅した心臓の画像診断の決定版となるテキストの改訂版。この間のモダリティの進化を踏まえて、掲載画像と記載内容を全面的に刷新した。心臓疾患の臨床に携わるすべての循環器科医、放射線科医、診療放射線技師にとって必読の1冊。
目次はこちらから
タグキーワード
いま話題の記事
-
ピットフォールにハマらないER診療の勘どころ
[第22回] 高カリウム血症を制するための4つのMission連載 2024.03.11
-
「看護」とは何をする仕事なのか
中田 明子氏(専修大学人間科学部社会学科 専任講師)に聞くインタビュー 2026.04.14
-
サルコペニアの予防・早期介入をめざして
AWGS2025が示す新基準と現場での実践アプローチ寄稿 2026.03.10
-
VExUS:輸液耐性が注目される今だからこそ一歩先のPOCUSを
寄稿 2025.05.13
-
インタビュー 2025.10.14
最新の記事
-
対談・座談会 2026.04.14
-
寄稿 2026.04.14
-
対談・座談会 2026.04.14
-
「看護」とは何をする仕事なのか
中田 明子氏(専修大学人間科学部社会学科 専任講師)に聞くインタビュー 2026.04.14
-
寄稿 2026.04.14
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。





