- 医学
異種臓器移植は実現するのか
小林 孝彰氏に聞く
インタビュー 小林孝彰
2023.11.06 週刊医学界新聞(通常号):第3540号より

1997年の臓器移植法施行から四半世紀が経過した。依然としてドナー不足の現状に大きな変化はなく,海外での臓器移植を無許可で斡旋したとして,NPO法人が摘発された事件は記憶に新しい。そうした状況下,かねて研究が進められてきたブタの心臓や腎臓を用いた異種臓器移植研究の成果が,米国を中心に立て続けに報告されている。臨床応用に向けてさまざまなハードルが考えられる中,果たして異種臓器移植は実現し得るのか。国際異種移植学会会長を務めるなど,異種移植研究に長年尽力してきた小林孝彰氏に現在地を聞いた。
米国で報告された異種臓器移植研究の成果に思うこと
――2021年末,米ニューヨーク大学で2例,アラバマ大学で1例のブタ腎臓移植が脳死患者に実施され1, 2),22年1月には同じく米国のメリーランド大学でECMOが装着された同種移植不適応の末期心不全患者に対してブタ心臓移植が行われました。ブタ心臓移植の例では,移植後60日間生存したと報告されています3, 4)。また本年9月には同大学で2例目のブタ心臓移植が成功したとの発表がありました。長年,異種移植研究に携わってきた小林先生の目から見て,相次いで発表された成果を受けての率直な気持ちを教えてください。
小林 いずれも異種移植研究に大きなブレイクスルーをもたらした成果と言えます。その一方で,いち早く実績を出したいとの研究者の気持ちが前面に出過ぎている印象を受けたのが本音です。移植の実施に当たって開示された情報も限定的であり,移植される患者として本当に適格だったのかと疑問を抱きました。
――どのような点からそう考えられるのですか。
小林 私は腎移植外科医ですのでブタ腎移植例に関して意見を述べます。通常,脳死状態になってから数日経過すると,ホルモンバランスや凝固系が乱れ,炎症も各部位に発生し,その影響で大抵の場合が心停止に至ります。米アラバマ大学で施術された患者の状態を詳細に追うと,移植術前(脳死判定5日後)の時点で凝固系が乱れていたことが明らかになっています。そうした状態では全身管理をされていても,すぐに血栓が発生するため長くは持ちません。そのため凝固系の乱れが脳死状態で起こったのか,異種臓器移植後の免疫反応によって起こったのかがわからない。つまり,脳死状態がどれほど異種臓器移植に影響を与えたのかが明らかにできないのです。しかも,3日間という限定付きの実施です。
このような悪条件の中で実施して,もしも結果が芳しくなかったらどうするのか。危険な研究とレッテルを貼られてしまうと本領域の研究全てにストップがかかる可能性すらあります。彼らのような勇気あるパイオニアたちが医学を発展させてきたとの事実はあるものの,今はもうそういう時代ではない。多施設が足並みをそろえていかに協力できるか。人類の未来を左右する研究だからこそ,プロセスを全て公開し,透明性を確保すべきと感じました。
異種臓器移植研究の歩み
小林 異種臓器移植研究の歴史は古く,免疫抑制剤の使用によるヒトの同種移植の成功を背景に,霊長類からの異種移植も数多く実施されるようになりました。1963~64年にかけてはチンパンジーからの腎移植5)やヒヒからの腎移植6)が行われています。また心臓7),肝臓8)においてもチンパンジーの臓器を用いた移植が行われました。しかしながら,多くは数時間から数日で機能廃絶に陥っています。
そうした時代を経て,免疫抑制療法の発展によって移植医療が定着し始めた1980年代後半においては移植臓器の需要が増加したことから,問題解決に向けた異種臓器移植への期待がさらに高まりました。1984年にはヒヒからの心臓移植9),93年には肝移植10)が行われ,それぞれ20日,70日生着したと報告されています。一方で,倫理的問題,感染症の危険性から霊長類を用いた移植は望ましくないとされ,ブタを用いた異種臓器移植が検討されるようになったのです。
――なぜブタが選ばれたのですか。
小林 ヒトに近い霊長類からの移植と異なり,ブタからの臓器移植では移植臓器が拒絶される超急性拒絶反応の存在が障壁ではあるものの,解剖学的,生理学的,血液生化学的にヒトに比較的近いとされ,繁殖能力が高く,妊娠期間も短いことから安定的に供給可能という点で優れています。また長年食用として扱われており,動物愛護的な問題も少ない。さらに比較的狭い飼育スペースで病原性微生物フリーの状態での管理が可能という点も理由として挙げられています。そうした可能性から,1994年に初めて遺伝子導入動物の作出技術がブタに応用され11),2002年に主要異種抗原であるαGal抗原の生成酵素であるα1,3 galactosyltransferaseをノックアウトしたブタが作出されました12)。けれどもその頃に一度,異種臓器移植研究の波が世界的に途絶えています。実現に向けて励んでいた研究者たちが当時を暗黒な日々と回顧するほどです13)。
――何らかの問題が発生したのでしょうか。
小林 培養細胞レベルではありますが,ブタの内在性レトロウイルス(PERV)がヒト細胞に感染することが報告され14),未知の感染症への対策に関して十分な議論を行う必要性が生じたからです。さらに,これらの遺伝子組換えブタを用いても拒絶反応を克服できず,臨床応用できないと判断され,異種臓器移植研究に投資をしていた企業の多くが撤退してしまいました。その後,ゲノム編集技術が登場して,ようやく風向きが変わり始めた。短期間で多種類の遺伝子を改変したブタの作出(図)15)が可能になり,PERVフリーのクローンブタが作出されるようになりました16)。現在では,10か所を改変したブタが作製され,冒頭に紹介した異種臓器移植の事例にも用いられたとされています。
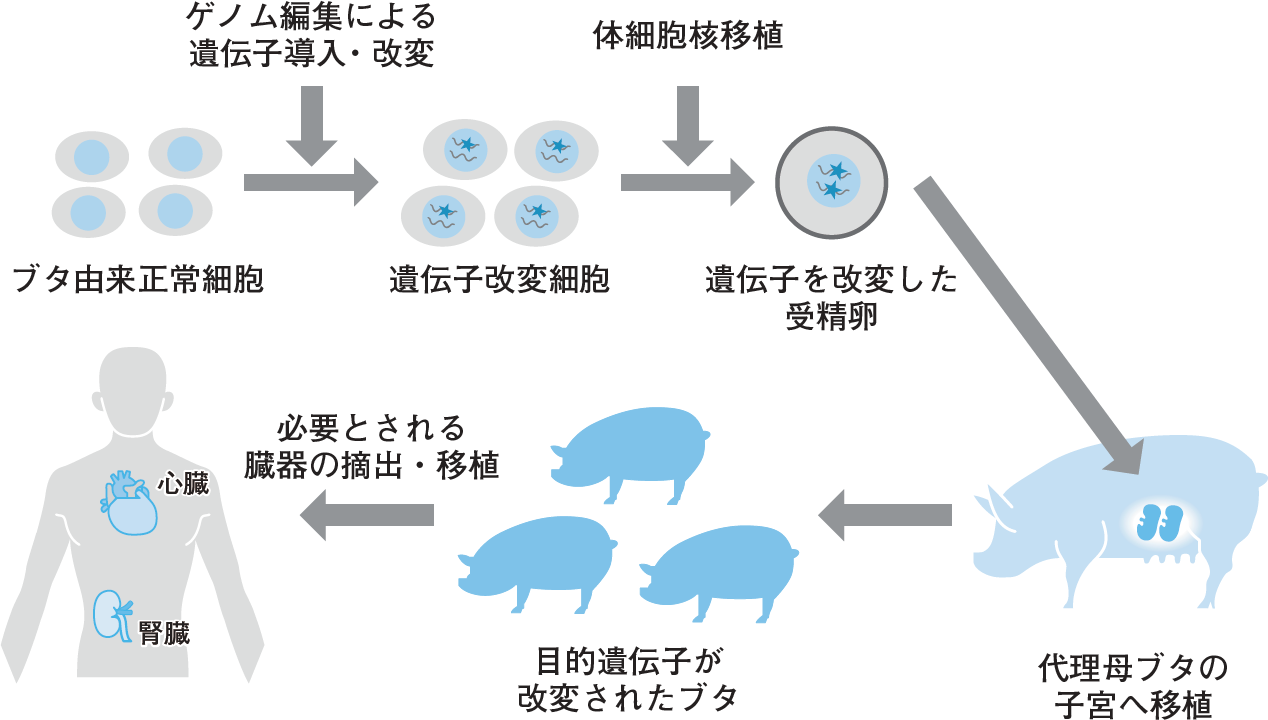
培養体細胞に対して遺伝子導入や遺伝子ノックアウトなどの変化を加え,遺伝子改変した細胞核を作製。得られた細胞核からクローン胚を作製し,代理母ブタへ移植,出産によって必要に応じた遺伝子改変ブタを作出する。
動物実験での限界
小林 一方で,今取り組まれている異種臓器移植研究が,先ほど紹介した2000年代前後の暗黒時代の二の舞になる可能性もあります。米国で報告が相次いでいるのも,企業からの資金面でのバックアップが潤沢にあるからです。すなわち企...
この記事はログインすると全文を読むことができます。
医学書院IDをお持ちでない方は医学書院IDを取得(無料)ください。

小林 孝彰(こばやし・たかあき)氏 愛知医科大学医学部外科学講座腎移植外科 教授
1985年名大医学部卒。西尾市民病院,安城更生病院,愛知県がんセンターで研修。移植外科医を志し,名古屋第二赤十字病院(当時)で研鑽を積む。移植医療について学ぶため94年米オクラホマ州のバプテストメディカルセンターへ留学。抗体に関する研究に携わる中で異種移植にも関心を持つようになる。95年に帰国し,名大医学部第二外科医員としてABO血液型不適合腎移植を手掛ける傍ら,超急性拒絶反応を防ぐためのαGalに関連した霊長類やブタを用いた異種移植研究を開始する。同大大学院医学系研究科移植免疫学寄附講座教授を経て,2015年より現職。13~15年にかけて国際異種移植学会会長を務め,現在は日本異種移植研究会世話人。25年には日本移植学会総会の大会長を務める。
いま話題の記事
-
あせらないためのER呼吸管理トレーニング
[ミッション7] マスク換気デバイスと友達になろう!連載 2026.05.12
-
VExUS:輸液耐性が注目される今だからこそ一歩先のPOCUSを
寄稿 2025.05.13
-
対談・座談会 2026.05.12
-
ピットフォールにハマらないER診療の勘どころ
[第22回] 高カリウム血症を制するための4つのMission連載 2024.03.11
-
実際どうなの? 糖尿病診療のココが知りたい
[第1回] 血糖悪化,どう考えて,どう動く?連載 2026.05.12
最新の記事
-
対談・座談会 2026.05.12
-
生涯を通じて女性のQOLを維持・向上する
産婦人科4本目の柱「女性医学」対談・座談会 2026.05.12
-
Sweet Memories
揺れながら進む,あなたの一歩に意味がある寄稿 2026.05.12
-
デジタル撮像とAIが切り拓く,細胞診の新たな地平
新田 尚氏(株式会社CYBO 代表取締役社長)に聞くインタビュー 2026.05.12
-
そのとき,研修医と指導医は何を考えているのか
麻酔科における「時間の流れ」と「思考の進め方」寄稿 2026.05.12
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。
