研究データの品質管理で不正を防ぐ?(後編)
研究公正のパラダイムシフトをめざす
寄稿 飯室 聡
2021.12.20 週刊医学界新聞(通常号):第3450号より
前編(3447号)では,研究への疑義に対して研究者が適切に対応できない原因を説いた。すなわち研究者は,FFP(研究不正)だけではなく,QRP(好ましくない研究活動)を加えたFFP/QRPに対処する必要があるということである。後編ではFFP/QRPの発生機序の観点からデータ管理の基本的な考え方について検討し,最終的には従来の研究公正からの転換を提示する。
「機会」を減らすことでFFP/QRPの発生を抑止する
以下では著者が研究代表者を務める2つの研究での議論を基に話を進める。1つは2018年度から2年間実施されたAMED研究公正・法務部の事業「研究データの質向上の指導者育成プログラム開発」。この一環で,現在「研究データの質向上の指導者育成研修事業」として年に数回の講習会を開催している。もう1つは2020年度後半より進行しているJST/RISTEXの「科学技術イノベーション政策のための科学研究開発プログラム」における「研究公正推進政策のための電子ラボノート実装ガイドライン作成を通したガバナンス研究」である。この研究では電子ラボノート実装実験を通じてラボにおけるデータの追加可能性・再現可能性を検討し,プロセス管理による研究の公正性の担保をめざしている。電子ラボノートはそのためのツールの1つとして位置付けられる。
◆なぜ不正(FFP/QRP)が発生するのか?
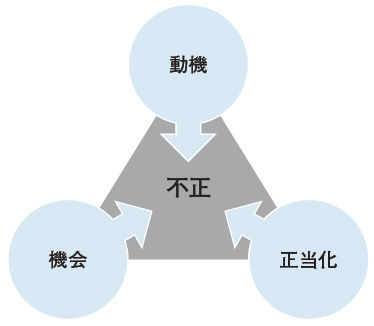
上記の研究の要点の1つは,FFP/QRPを検討する際にそれらの「発生機序」から考える重要性である。これに当たって,われわれ研究グループは「不正のトライアングル理論」(図)1)を用いた。この理論は1953年に米国の犯罪心理学者Donald R. Cresseyが提唱した古典的理論だが,現在でも企業不正等への基本的な分析ツールとして用いられている。これは図に示すように,「不正の成立には動機・機会・正当化という3つの要素が必要」とする極めて単純な理論である。企業不正(横領)を例に考えてみよう。不正は借金があるなどの「動機」と,会計担当者が監査担当者を兼任しているなどの「機会」の状況があるだけでは起こらない。そこに「一時的に借りるだけ」などの「正当化」が加わって,初めて不正(横領)が成立する。
表では企業不正・医療過誤・FFP・QRPを対比している。まず企業不正と医療過誤を対比してみよう。故意に引き起こされる企業不正と異なり,医療過誤は医療従事者の過失(ミス)に基づく。そのため「動機」と「正当化」は存在しないが,「機会」があるために現実には医療過誤が発生し得る。例えば注射ミスでは,医療従事者には「動機」と「正当化」はない。しかし注射の際に周囲がチェックする手続きが存在しないことが「機会」となりミスにつながる。故意に行う不正と異なり,「機会」があるだけで結果としての医療過誤が起こり得るのである。

表のFFPとQRPではどうだろうか。FFPには明確な「動機」と「正当化」がある。QRPには「動機」はないが「正当化」はあり得る。注目すべきは両者ともに必ず「機会」があること,つまり「プロセス管理/データ管理がブラックボックスになっている」点である。これを可能な限り明確化し「機会」を減らすことで,FFP/QRPの発生はある程度のレベルで抑制が可能になる。
◆研究公正の両輪としての研究倫理教育とプロセス管理
研究倫理の立場からのFFP/QRPに対する介入ポイントは,「動機」(メリ...
この記事はログインすると全文を読むことができます。
医学書院IDをお持ちでない方は医学書院IDを取得(無料)ください。

飯室 聡(いいむろ・さとし)氏 国際医療福祉大学未来研究支援センター 副センター長/同大大学院医学研究科公衆衛生学専攻教授
1995年東大医学部保健学科卒,99年同大医学部医学科卒。博士(医学)。同大病院などで研修後,同院臨床研究支援センター助教,東京女子医大先端生命医科学研究所准教授などを経て,2019年より現職。20年より国際医療福祉大大学院教授,21年より同大研究倫理支援室室長を兼任。
いま話題の記事
-
医学界新聞プラス
[第1回]自分だけの聴診器選びと,音を逃さない当て方のキホン
Dr.いっしーの聴診レッスン連載 2026.04.03
-
連載 2026.03.30
-
ピットフォールにハマらないER診療の勘どころ
[第22回] 高カリウム血症を制するための4つのMission連載 2024.03.11
-
VExUS:輸液耐性が注目される今だからこそ一歩先のPOCUSを
寄稿 2025.05.13
-
医学界新聞プラス
[第1回]抗菌薬を理解するためのスタートライン
『知識がつながる抗菌薬――まるわかり感染症診療』より連載 2026.04.02
最新の記事
-
対談・座談会 2026.04.14
-
寄稿 2026.04.14
-
対談・座談会 2026.04.14
-
「看護」とは何をする仕事なのか
中田 明子氏(専修大学人間科学部社会学科 専任講師)に聞くインタビュー 2026.04.14
-
寄稿 2026.04.14
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。
