HIF;Highly Involved Factor(広田喜一)
寄稿
2019.12.02
【特別寄稿】
HIF;Highly Involved Factor
|
 |
| 広田 喜一(関西医科大学附属生命医学研究所侵襲反応制御部門学長特命教授) |
アルフレッド・ノーベルの命日である12月10日に毎年行われるノーベル賞授賞式がいよいよ1週間後に迫ってきた。2019年のノーベル医学・生理学賞は「細胞の酸素利用度の感知と応答の仕組みの解明」に貢献した英米の3氏に贈られる。3氏の研究は,生体に不可欠な酸素をいかに感知し,応答するかを解明したことで,酸素濃度が与える生理学的な影響を理解する上で基盤となるものだ。貧血やがんなどの疾患へ立ち向かう新たな戦略の種となったことも評価された。
細胞が酸素に応答する仕組みの根幹を担う遺伝子の単離を行ったGregg L. Semenza氏(米ジョンズ・ホプキンス大)の研究室で客員教授としてその後の関連研究に携わった広田喜一氏が,これらの知見の医学的意義について本紙に寄稿した。
(本紙編集室)
スウェーデンのカロリンスカ研究所は10月7日,2019年のノーベル医学・生理学賞を「細胞の酸素利用度の感知と応答の仕組みの解明」への貢献を理由に,米ハーバード大ダナ・ファーバー癌研究所のWilliam G. Kaelin, Jr博士,英オックスフォード大・フランシス・クリック研究所のSir Peter J. Ratcliffe博士,米ジョンズ・ホプキンス大のGregg L. Semenza博士へ授与することを発表しました。本稿では新聞,雑誌で概要が報告されているこの分子システムの詳細については他に譲り,この受賞のパースペクティブを解説したいと思います。
ポストEPO製剤としての期待
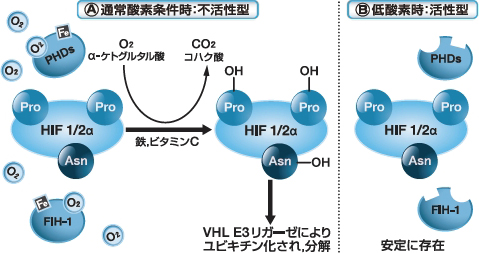
受賞研究をより具体的に述べると,1980年代の終わり頃にその端緒が見いだされるエリスロポエチン(erythropoietin;EPO)の発現維持・誘導の分子機序について説明する因子として単離された低酸素誘導性因子(hypoxia-inducible factor;HIF)の発見と,その酸素分圧依存性の活性調節の分子機序の解明です(図1)。ここで重要な役割を果たすのは酸素濃度依存的な酸素添加酵素です。これらを「低酸素センサー」と考える研究者もいます。HIFのαサブユニット(HIF-α)のプロリン残基の水酸化を担う3種類の酵素とアスパラギン残基の水酸化を担う1種類の酵素が現在知られています。アスパラギン残基の水酸化を担う酵素はFIH-1と命名され,この分子の遺伝子単離には筆者もSemenza氏の研究室員として参加しました。
これらの研究結果は,腎性貧血の治療薬として「ポストEPO製剤」と呼ばれ期待を集めています。本邦でも2019年9月に1剤目が承認された腎臓領域の新しいタイプのHIF活性化薬(roxadustat,vadadustat,daprodustat,molidustat)にも応用されています。『The New England Journal of Medicine』誌で先頃公刊された論文によれば,透析導入された患者の貧血治療において,EPO製剤と比較してのroxadustatの非劣性がすでに示されています。こうした臨床医学への直接の貢献も今回の授賞を後押ししたと考えられます。
腎臓間質に存在する特別な細胞でEPOの産生に貢献している転写因子はHIF-1でなくHIF-2であると現在では考えられています。HIFはトランスフェリンやトランスフェリン受容体,セルロプラスミン,ヘプシジンなどの発現調節に直接・間接に関与することが示されています。これらのことから,HIF-α水酸化酵素阻害薬はEPOのみならず鉄代謝を改善することで貧血の改善に貢献すると言えます。
遺伝性の多血症のいくつかはこのパスウェイの分子の遺伝子異常で説明できます。Chuvash polycythemia(常染色体劣性遺伝)はHIF-αタンパク質のユビキチン化酵素として機能しその分解に関与するVHLの,PHD2 erythrocytosis(常染色体優性遺伝)はHIF-αプロリン水酸化酵素の一つであるPHD2の異常です。さらにHIF-2α erythrocytosis(常染色体優性遺伝)はHIF-2αの遺伝子異常で発症する多血症です。ちなみにChuvash polycythemia発症の分子機構の解明には筆者も参加しました。
酸素のバランスを感知し,酸素利用モードを調整する
このようにHIFはEPOの発現調節に多重に関与する因子ですが,さらに重要なことは,HIFをめぐる一連の研究が,生体における酸素の役割についての考え方つまり酸素観を変えた点にあります。酸素はヒトの生命の維持に必須な分子です。この観点から酸素は細胞のATP産生に必須な分子であり,その欠乏によるエネルギー不足により生体機能の維持が不可能となるというスキームが想定されます。その欠乏は細胞死,生体機能の失調を経て個体の死に至る,と考えられてきました。
しかし,このような古典的な酸素観はここ20年くらいの研究により完全に見直されています。そもそも酸素は,多種の組織・臓器で構成される脊椎動物のような高等生物ではむしろ常に「不足」しているのです。酸素は生命維持に必須な分子であるにもかかわらず,私たち哺乳類は酸素を体内で生合成する仕組みを持ちません。それ故生体はその必須分子の不足,つまり低酸素に応答する仕組みを進化的に構築して身体の統合の維持に積極的に利用してきたとの考え方が主流となりました。
HIF-1は「低酸素」で活性化しますがこの「低酸素」という言葉はそもそも曖昧です。多くの培養細胞では培養環境の酸素濃度を5%まで低下させるとHIF-1αタンパク質の発現が確認されるようになります。しかしこの原則が当てはまらない細胞も存在します。
また,逆説的に思えますが,細胞は低酸素に暴露されると活性酸素を発生します。この仕組みを利用してHIF-1をあらかじめ活性化することで,低酸素環境下での活性酸素の発生を抑制することができます。これらの性質を利用して虚血再灌流傷害の軽減戦略にHIF-1の活性化が利用できるという研究も存在します。
さらに,HIF-1活性化へのネガティブフィードバック機構が存在します。HIF-1の活性化が持続すると,HIF-1活性を抑制する機構が発動します。
このようにHIF-1は,酸素不足で活性化するのみならず,細胞の酸素利用モードを積極的に調節する役割を担っています。酸素利用において,その供給の不足だけでなく需要の側面を同時に最適化することで生体は恒常性を維持しているのだという現代的な酸素観の成立に今回のノーベル賞の業績が果たした役割は大きいと言えます。
HIFは生体の酸素利用とさらに広くかかわっています。呼吸器は,赤血球中のヘモグロビンに酸素を移行するための場を提供する肺や,血液中の酸素分圧を感知する神経上皮細胞などで構成されます。循環器は,酸素運搬媒体である赤血球,運搬ポンプである心臓,その運搬経路である血管で構成されます。これらシステムの調和の取れた発達と維持のためには,おらく数千の遺伝子の調和の取れた発現が必要です。
このような遺伝子発現をつかさどる転写因子がHIFです(図2)。低酸素で発現が変化する遺伝子のうち2千個程度(全遺伝子の約10%)はHIF-1によりその発現が制御されていることを示す報告があります。このような現象への広く決定的な関与からHIFをhighly involved factorだとSemenza博士はかつて呼びました。
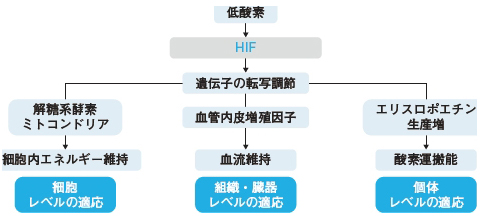 |
| 図2 HIFと生体の酸素代謝 |
| 転写因子ネットワークと低酸素応答HIFに依存した遺伝子応答は,生体の低酸素応答の重要な要素であり,ネットワークを形成している。細胞,組織・臓器,個体レベルでの応答が存在し,各レベルで個々の細胞の応答の総和として低酸素応答が現れる。このネットワークのキー転写因子としてHIFが同定された。HIFは核を持つ全ての細胞に存在し,細胞が暴露される酸素分圧に依存して活性化が決まり,細胞・組織特有の因子により活性化が修飾を受けることも知られている。 |
これらの知見により網膜血管が異常増殖する未熟児網膜症の発症,逆に透明であるべき角膜での血管新生抑制の分子機序なども説明することができます。さらに,持続的な低酸素血症を引き起こす先天性心疾患などでは肺高血圧が起こる一方,睡眠時無呼吸症候群は間欠的な低酸素血症と再酸素化を伴い体血圧の上昇を招きます。Semenza博士らはこの違いを間欠的な低酸素―再酸素化によって発生する活性酸素がHIF-1とHIF-2の活性バランスを撹乱する機序で説明できるとの論文を発表しています。
HIFの安易な活性化・抑制には懸念も
今回のノーベル賞に関する新聞などの報道ではHIFのがんへの関与が強調されています。一方,がん細胞におけるHIF-1,HIF-2の活性化は酸素分圧変化のみでは説明ができません。
一例としてVHLを見てみましょう。VHLはフォン・ヒッペル―リンダウ病の原因遺伝子です。腎臓がんなどではがん抑制遺伝子として知られ, VHLタンパク質の欠失や機能異常が臨床的に高頻度で観察されます。この欠失は酸素分圧に関わらずHIF-1,HIF-2の活性化をもたらします。また乳がんをはじめとしたいくつかのがんで高発現している場合がある受容体型チロシンキナーゼHER2の刺激は,やはり酸素分圧とは無関係にHIF-1の活性化をもたらします。
がん以外にも,妊婦に起こる子癇の発症機序,さらに妊孕性へのHIFの関与があると主張する有力な論文もあります。紫外線照射,ウイルス感染やムスカリン性アセチルコリン受容体への刺激,さらに喫煙によってもHIFは活性化します。これらの状況におけるHIFの活性化は,実は低酸素による活性化とは異なる機序で起こると示されています。
HIFは生体内のさまざまな種類の細胞・組織でさまざまな役割を担っています。人為的に活性化・抑制を行うと生体内でのバランスが破壊されます。がんの治療に応用するとすれば,がん組織を標的とする適切なドラッグデリバリーシステムの開発が必須です。単純にHIFを阻害する薬剤を全身投与すると,EPOの発現抑制や鉄代謝の撹乱が起こり,重篤な貧血などが発症する可能性があります。逆に,がん細胞でHIFのさらなる活性化をもたらす可能性のある腎性貧血の治療薬を担がん患者に使用することの適否はすでに議論の俎上に上がっています。
*
今回の受賞者は3人とも医師資格を持つ基礎研究者です。つまりphysician scientist,MD-scientistと呼ばれる人たちです。Kaelin氏は泌尿器科,Ratcliffe氏は腎臓内科,そしてSemenza氏は小児科が出自です。
筆者も麻酔科の医師として,米ジョンズ・ホプキンス大のSemenza研究室に1999年の8月から2002年の2月まで京大からの訪問教授として参加しました。当時,彼はまだ准教授で小児科医としてのポケットベルを携帯して臨床業務も行っていました。
筆者が彼の研究室に参加した時はHIF-1のcDNAの単離が終わった時点で,HIF-1活性化機序の詳細を解明する基礎研究に加えて,がんと虚血再灌流傷害克服のための臨床的な研究への助走中でした。ポスドク2人,テクニシャン1人,医学部受験をめざすインターン1人に学生1人のこぢんまりとした所帯でした。当時筆者が所属していた京大麻酔科の研究室より小さく,ここでHIF-1のcloningに成功したとはにわかには信じられませんでした。
Semenza博士はたびたび来日しています。つい先日,9月26日には日本癌学会での講演の後,ダブルヘッダーで関西医大にて大学院生を対象とした講演「Advice for a young scientist」を行ってもらいました。本人も話していましたが,このようなタイトルで講演を行うことは珍しく,というより今までなく,今回はたってのお願いとして聞き届けていただきました。
1. Search and research
2. A good mentor (or 2 or 3) matters
3. Have a plan
4. Embrace serendipity
5. If you ask for help, you will get it.
6. If you don't ask for help, you won't get it.
7. Examine primary data from “failed” experiments
8. Technical courage and collaboration
9. What is science?
10. The best job in the world
この10項目について彼のHIF-1研究の進行に合わせて熱弁を振るってくれました。「若い研究者へのメッセージになるような講演を」とお願いしたら,スライドを最初から作りなおす必要があると難色を示されたのですが,最終的には筆者の依頼通りのタイトルで講演をしてもらえ,無理を承知で頼んでよかったと思いました。
その後彼の研究室に在籍した日本人研究者の同窓会を彼を交えて枚方市駅前で行いました(写真)。
 |
| 写真 Semenza研究室メンバーのリユニオン(後列中央が筆者,前列中央がSemenza氏) |
現在Semenza研究室には日本からの留学生はいません。皆さんも少しの勇気を持って彼の研究室に飛び込んでみてはいかがでしょうか。Greggがポスドクに期待することはそう多くありません。基本的な研究手技を身につけていること,正直であること,研究室の皆と仲良くできることだけです。『Nature』『Cell』『Science』などへのpublicationは必要ありません。Greggの研究室で私は,研究のアイデアの出し方,またその進め方から,研究室ミーティングの進め方まで多くを学びました。日本人研究者はいつでも大歓迎だと彼も話しています。
「ノーベル賞に届くといいね」と同窓会のあと皆で話しましたが本当に「キター」ので驚きました。
 ひろた・きいち氏
ひろた・きいち氏
1988年京大医学部卒。臨床研修を経て96年同大大学院医学研究科博士課程単位修得および研究指導認定,97年に博士号(医学)取得。同大助手,米ジョンズ・ホプキンス大客員教授,産総研主任研究員,京大講師,准教授,関西医大准教授を経て,2016年より現職。
いま話題の記事
-
忙しい研修医のためのAIツールを活用したタイパ・コスパ重視の文献検索・管理法
寄稿 2023.09.11
-
人工呼吸器の使いかた(2) 初期設定と人工呼吸器モード(大野博司)
連載 2010.11.08
-
連載 2010.09.06
-
事例で学ぶくすりの落とし穴
[第7回] 薬物血中濃度モニタリングのタイミング連載 2021.01.25
-
寄稿 2016.03.07
最新の記事
-
医学界新聞プラス
[第4回]脆弱性骨盤骨折
『クリニカル・クエスチョンで考える外傷整形外科ケーススタディ』より連載 2024.04.26
-
医学界新聞プラス
[第3回]わかりやすく2つの軸で分類して考えてみましょう
『心理社会的プログラムガイドブック』より連載 2024.04.26
-
医学界新聞プラス
[第1回]平坦な病変 (1)色調の変化があるもの
『内視鏡所見のよみ方と鑑別診断——上部消化管 第3版』より連載 2024.04.26
-
医学界新聞プラス
[第1回]心エコーレポートの見方をざっくり教えてください
『循環器病棟の業務が全然わからないので、うし先生に聞いてみた。』より連載 2024.04.26
-
医学界新聞プラス
[第1回]バルーン閉塞下逆行性経静脈的塞栓術(BRTO)
『IVRマニュアル 第3版』より2024.04.26
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。