飛躍するオルガノイド研究
対談・座談会 佐藤 俊朗,武部 貴則
2021.10.18 週刊医学界新聞(通常号):第3441号より

「幸運の女神は,常に準備している人にのみ微笑む」と,近代細菌学の祖であるPasteurは言った。科学の世界では度々,偶然の発見が歴史的な研究報告となる場面がある。しかしその発見を成果としてつかめるのは,周到な準備を行い,偶然を見逃さない鋭い観察力と執着心を持つ者だけだ。
世界で初めて腸管オルガノイドの培養に成功した佐藤氏1)と,同じくヒト肝臓オルガノイドを確立した武部氏2)も,まさに観察力と執着心を持ってチャンスをつかんだ2人だ。「生きた小さな臓器(organ)のようなもの(-oid)」を意味するオルガノイド(organoid,MEMO・図)は,生物学と医療を大きく発展させる鍵となる。本領域に革命を起こした2人が語る,オルガノイド研究の面白さと期待される医療の形とは。
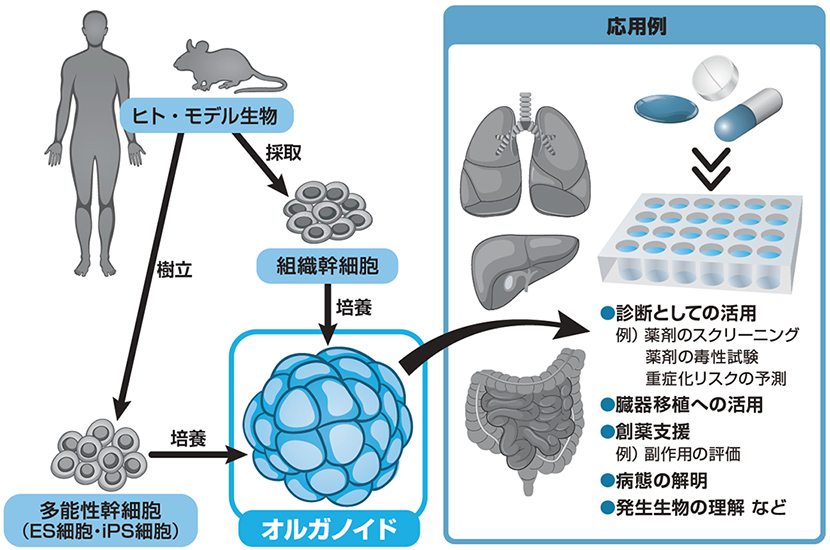
ヒトやモデル生物から,複数の組織幹細胞または多能性幹細胞を採取または樹立し,適切な条件下で培養することで作られる。作られたオルガノイドは,患者一人ひとりに最適な医療を提供するMy Medicine の実現に向けた応用などが期待されている。
武部 オルガノイドに関連する原著論文は,研究が始まった20世紀全体で170本程度だったのに対し,2021年9月現在では累計2000本を超えています。オルガノイド研究が近年著しく発展した背景には,多能性幹細胞の発見を含む幹細胞生物学の進展があります。中でも2009年に佐藤先生が報告した,幹細胞を生体外で永続的に三次元培養する技術1)は,研究を加速させる大きな発見でした。どのようにして発見に至ったのでしょうか。
佐藤 一つひとつ想定しながら創り上げたというよりは,偶然「やってみたらできた」というのが正確です。その頃私は,生体外で増殖・維持させるのが難しいために機能解析が困難とされていた腸管上皮幹細胞の培養方法を模索していました。5年ほど失敗が続いた後,上皮幹細胞を培養する鍵となる3種類のタンパク質を培養液に加えたところ,単一の腸管上皮幹細胞がシャーレの中で3次元構造物へと成長することを発見したのです。その構造物は中空の球状体で,絨毛や陰窩といった腸管特有の構造を有していたので,まるで小さな腸が育っているように見えました(写真)。このように,全く予期せず「オルガノイド」ができたわけです。
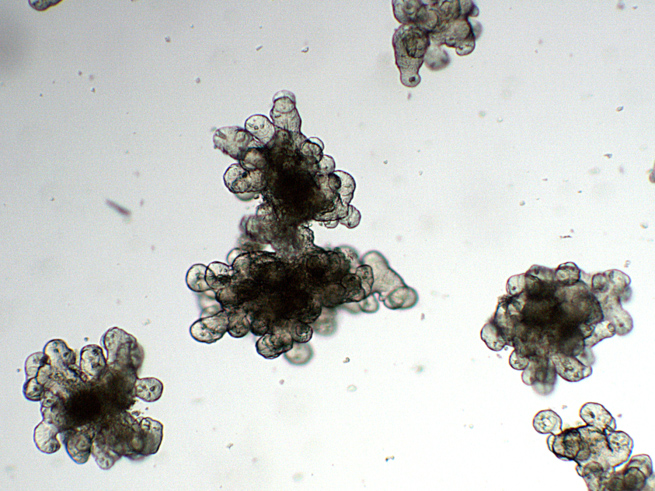
絨毛状の上皮と陰窩状の構造によって裏打ちされた,0.5mmほどの中空の球状体が観察できる。
武部先生は医学部を卒業した2011年から肝臓の研究を始め,同年にはヒト肝臓オルガノイドの培養に成功されています。そもそもどのような経緯で研究を始められたのですか?
武部 きっかけは医学生の頃,留学先の米国の病院で多くの肝不全患者がドナー不足で亡くなる様子を目の当たりにした経験です。臓器再生の研究の道に進めば多くの患者を救えると考え,大学卒業後は臨床研修をせず,研究室で肝臓組織を創るために試行錯誤していました。
佐藤 肝臓の再生研究は当時から多くの研究者が取り組んでいました。その中で武部先生は,iPS細胞だけではなく血管内皮細胞や線維芽細胞など複数の細胞と混ぜ合わせて培養するユニークな方法2)を開発されましたね。
武部 複数の細胞を細胞培養には本来適さない培養皿であるローアタッチメントプレートであえて培養したところ,翌日5 mmほどに成長した細胞の塊が生まれていました。さらにその塊は生体内の肝臓と同様,3次元的な血管を有しタンパク産生や薬物代謝などの機能を果たしたのです。私も佐藤先生と同様に「やってみたらできた」ので,できた塊が後に「オルガノイド」と呼ばれるとは思っていませんでした。
「やってみたらできた」に後付けで論理を組み立てる
佐藤 iPS細胞は原理的にあらゆる体細胞に分化できますが,特定の細胞に正確に分化させるためには,何段階もの発生段階をシャーレの中で再現しなければなりません。事前にある程度の予測は可能であるものの,大抵は思いもよらない要素が必要となります。武部先生のように,加える要素が意外であるほど発見としての価値は大きくなる一方で,成功の要因を論文として論理的に落とし込む作業は難しかったのではないでしょうか?
武部 ええ。特に私の発見は先行研究のない報告だったため,論文が厳しく査読されました。「論理的に説明できない部分がある」との指摘を多数受けて一つひとつ対応した結果,4枚ほどの論文に対して論文をサポートするデータ資料は200枚近くとなりました。ご存じの通り,科学の世界ではしばしば,研究対象を細かく分析して原理を説明する要素還元的な考え方が重視されます。現象的なアプローチを取る私の研究は受け入れられにくいものだったのです。
佐藤 テクノロジーが発展した今でこそ,複雑な事象を包括的に理解しようと試みる研究スタイルが珍しくなくなりつつあります。しかし当時はシンプルな要素還元的アプローチが最も有効と考えられていました。例えば,特定の遺伝子を欠損させたノックアウトマウスの形質を解析して遺伝子の意味を一つずつ明らかにする。こうして積み上げられた理論を基に仮説を立て,実証していくのが一般的でした。「やってみたらできた」で実績を重ねるオルガノイド研究とは真逆のスタイルです。
武部 論文掲載となる直前に先輩研究者からは「お前の研究は汚い!」と怒られました。しかし私にとってその言葉は「今後このスタイルを続けることで,自分らしい研究ができるんだ」との気付きを得る指摘で,かえってやる気が出ました(笑)。このスタイルこそがオルガノイド研究の面白さだと思っています。
佐藤 サイエンスというよりアートに似た研究領域ですよね。どの細胞を組み合わせて,何の刺激を与えてどういう培地で培養するか。多様な条件での試行錯誤を繰り返しながらもささいな変化は決して見逃さず,緻密な実験をしつこく続ける。そうして偶然できたオルガノイドを前に,次は「なぜできたのか」を追究するのです。
武部 後付けで原理を解明し論理を組み立てる過程は好奇心が刺激されます。さらに近年,オルガノイドの原理を明らかにしていく中で,これまで明かされていなかった生物学のピースも集まり始めています。とりわけ影響を与えているのは発生生物学でしょうか。
この記事はログインすると全文を読むことができます。
医学書院IDをお持ちでない方は医学書院IDを取得(無料)ください。

佐藤 俊朗(さとう・としろう)氏 慶應義塾大学オルガノイド医学 教授
1997年慶大医学部卒。同大病院での臨床研修後,臨床業務と並行して同大大学院で炎症性腸疾患の研究を行う。その後,博士研究員として米ストワーズ医学研究所や蘭ユブレフト研究所で腸の再生の研究に従事。帰国後は慶大消化器内科で消化器がんの研究にも携わり,2016年より慶大消化器内科准教授。18年より現職。

武部 貴則(たけべ・たかのり)氏 東京医科歯科大学器官発生・創生学 教授
2011年横市大医学部卒,18年より現職。15年より准教授を務める米シンシナティ小児病院では研究基盤の開発,東京医歯大では主にオルガノイド実用化の方法を模索している。さらに19年に特別教授に就任した横市大では,デザインやコピーライティングなどの広告的視点を医療現場のコミュニケーションに取り入れる独自の学問領域「広告医学」の研究も進める。
いま話題の記事
-
対談・座談会 2026.05.12
-
VExUS:輸液耐性が注目される今だからこそ一歩先のPOCUSを
寄稿 2025.05.13
-
ピットフォールにハマらないER診療の勘どころ
[第22回] 高カリウム血症を制するための4つのMission連載 2024.03.11
-
サルコペニアの予防・早期介入をめざして
AWGS2025が示す新基準と現場での実践アプローチ寄稿 2026.03.10
-
あせらないためのER呼吸管理トレーニング
[ミッション7] マスク換気デバイスと友達になろう!連載 2026.05.12
最新の記事
-
対談・座談会 2026.05.12
-
生涯を通じて女性のQOLを維持・向上する
産婦人科4本目の柱「女性医学」対談・座談会 2026.05.12
-
Sweet Memories
揺れながら進む,あなたの一歩に意味がある寄稿 2026.05.12
-
デジタル撮像とAIが切り拓く,細胞診の新たな地平
新田 尚氏(株式会社CYBO 代表取締役社長)に聞くインタビュー 2026.05.12
-
そのとき,研修医と指導医は何を考えているのか
麻酔科における「時間の流れ」と「思考の進め方」寄稿 2026.05.12
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。
