生活習慣病におけるゲノム研究の進歩(久保充明)
寄稿
2011.02.28
【寄稿】
生活習慣病におけるゲノム研究の進歩
オーダーメイド医療の実現をめざして
久保充明(理化学研究所ゲノム医科学研究センター・副センター長)
過去10年間で飛躍的に進展したゲノム研究
2001年にヒトゲノムの約30億塩基の概要配列が決定されてから,10年が経過した。この間にヒトの疾患に関するゲノム研究は飛躍的に進んだ。特に,生活習慣病などのありふれた疾患の発症に関連する遺伝要因の解明が急速に進んでおり,すでに2型糖尿病では20か所以上,特定疾患でもあるクローン病では70か所以上の関連遺伝子が同定されている。
この爆発的な進展には,ヒトゲノムプロジェクトと国際ハップマッププロジェクトの成功から,ヒトゲノム研究の基盤情報が整備されたことが深くかかわっている。ヒトゲノムプロジェクトは,ヒトゲノムの約30億塩基を構成するA(アデニン),G(グアニン),C(シトシン),T(チミン)の4種類の塩基が,染色体上にどのような順番で並んでいるかを明らかにした。一方,国際ハップマッププロジェクトは,個々人の30億塩基の配列を比べた際に認められる1塩基の違い(SNP)のゲノム上の位置と,アジア人・アフリカ人・ヨーロッパ人の3人種における頻度をデータベース化した。これらの情報が迅速にホームページで公開されたことにより,ヒトゲノム全体を網羅的に調べ,疾患や薬剤の反応性に関連する遺伝子を探すゲノムワイド関連解析(genome-wide association study; GWAS)の手法が確立された。
生活習慣病のGWASを世界で初めて成功させたのが,理研の田中らである1)。氏らは2002年に,1000例を超える心筋梗塞患者と健常対照者について約10万か所のSNPを調べ,LTA遺伝子が心筋梗塞関連遺伝子であることを発見した。その後,SNPを大量高速に測定するSNPチップがアフィメトリクス,イルミナの両社から発売されたことにより,2007年以降,世界中の研究者がGWASを行うようになった。その結果,疾患,薬剤反応性,血液検査値,ニコチン依存性などさまざまな病態と関連する遺伝子群が多数報告されるようになり,ゲノム研究のゴールドラッシュ(または爆発)と呼ばれている(図)。
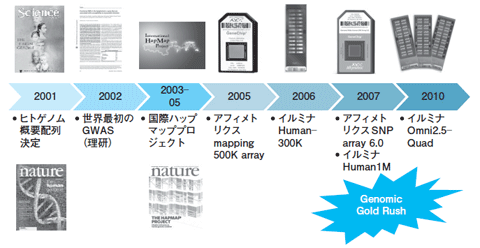 |
| 図 最近10年間におけるヒトゲノム研究の進展 |
GWASにより関連遺伝子の網羅的発見が可能に
ヒトゲノムの30億塩基の中から疾患に関連する遺伝子を同定するには,ゲノム上の個人ごとに異なるマーカーが必要である。現在,最も利用されているマーカーが前述したSNPである。その理由としては,SNPは1塩基のみの違いのため測定が容易であること,ゲノム上に高密度に存在するためマーカーSNPから推定される関連領域が非常に狭いことなどが挙げられる。現在,世界中で行われているGWASでは,このSNPをマーカーとして用い,ヒトゲノム全体をカバーするように50万から100万か所を測定する。得られたSNPの頻度を疾患群・対照群間で比較し,頻度に差があるSNPを探し出すことにより,そのSNPが存在するゲノム領域にある遺伝子を疾患関連遺伝子として同定する方法である。
生活習慣病関連遺伝子の発見
常染色体優性遺伝などの明らかな遺伝形式を示す疾患では,特定の家系について数百か所のVNTR(variable numbers of tandem repeats),マイクロサテライトをマーカーとして測定し,家系データと組み合わせるといった連鎖解析の手法により,多くの原因遺伝子が過去に特定されてきた。
この方法は,遺伝子の変異によりほぼ100%の確率で発症する遺伝性疾患では非常に有用であった。しかし,ゲノム上の塩基の違いが疾患の発症リスクにわずかに影響するのみである生活習慣病においては,連鎖解析の手法は有用ではなかった。また,生活習慣病の発症機序に関与する遺伝子群(例えば,高血圧におけるレニン・アンジオテンシン系の遺伝子)をターゲットとした候補遺伝子研究も過去盛んに行われたが,一致した結論は得られなかった。ところが,ゲノム研究の進展により,数千から数万例の患者群と対照群を用いた大規模なGWASが行われることとなり,次々と生活習慣病の関連遺伝子群が発見されている。興味深いことに候補遺伝子研究で検討された遺伝子の多くは,GWASでは関連が見られていない。
オーダーメイド医療の実現に向けて
生活習慣病の関連遺伝子一つひとつが疾患の発症に与える影響は,アルツハイマー病のAPOE遺伝子多型や加齢黄斑変性のCFH遺伝子多型などの例外を除き,ほとんどはオッズ比1.1-1.5と影響力は小さい。しかし,リスク遺伝子型を数多く持つ人は当然のごとく疾患発症のリスクが高い。また生活習慣病では,遺伝要因だけではなく,環境要因もその発症や進展に大きく関与する。したがって,個々人の遺伝要因(体質)を考慮した薬剤や治療法の選択,疾患の予防を実現していくためには,多くの症例を長期間追跡し,生活習慣病のリスク遺伝子型の集積がどの程度疾患の発症や進展に関与するかを明らかにする必要がある。さらに,喫煙・飲酒などの環境要因が個人の遺伝的リスクに与える影響を検討することにより,個人の遺伝要因に応じた効果的な予防法を見いだすことが可能となる。つまり,ゲノム研究から得られた膨大な生活習慣病の関連遺伝子の情報を医療へ応用するためには,大規模なゲノム疫学研究による評価が必要不可欠である。
*
今から150年以上前に,チャールズ・ダーウィンは遺伝的多様性が生物の進化・生存に重要であることを指摘した。ゲノム研究の急速な進歩により,われわれはこの概念を現実のデータとして理解できるようになりつつある。個人のゲノム情報を考慮したオーダーメイド医療が実現する日が,目の前に近づいている。
1)Ozaki K, et al. Functional SNPs in the lymphotoxin-alpha gene that are associated with susceptibility to myocardial infarction. Nat Genet. 2002; 32(4): 650-4.
 |
久保充明氏 |
いま話題の記事
-
心電図のレッドゾーン“ST 上昇”(その5)もしすべての誘導でST が上がっていたら(前編)(香坂俊)
連載 2011.09.12
-
事例で学ぶくすりの落とし穴
[第7回] 薬物血中濃度モニタリングのタイミング連載 2021.01.25
-
寄稿 2016.03.07
-
人工呼吸器の使いかた(2) 初期設定と人工呼吸器モード(大野博司)
連載 2010.11.08
-
連載 2010.09.06
最新の記事
-
医学界新聞プラス
[第3回]学会発表のスライド作成①
『医師による医師のためのChatGPT入門——臨床がはかどる魔法のプロンプト』より連載 2024.06.14
-
医学界新聞プラス
[第2回]「外来診療」を構造化する
『「卓越したジェネラリスト診療」入門――複雑困難な時代を生き抜く臨床医のメソッド』より2024.06.14
-
対談・座談会 2024.06.11
-
対談・座談会 2024.06.11
-
対談・座談会 2024.06.11
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。
