新年号特集「認知症に挑む」
MCI(mild cognitive impairment;軽度認知機能障害)の概念と
認知症予防としての生活習慣病対策が持つ可能性
荒井啓行1),古川勝敏2)(東北大学先進漢方治療医学教授1),助教授2))
認知症の定義
一般に,認知症とは「一度獲得された知的機能の後天的な障害によって,自立した日常生活機能を喪失した状態」と考えられている。実際,図に示すように,日常的な生活遂行機能は高齢になっても衰えることはなく,時間軸に概ね平行に推移すると考えられる。一方,認知症患者では明らかな右肩下がり現象が見られ,日常生活または社会生活機能の明らかな喪失をきたし認知症と判断されるようになる。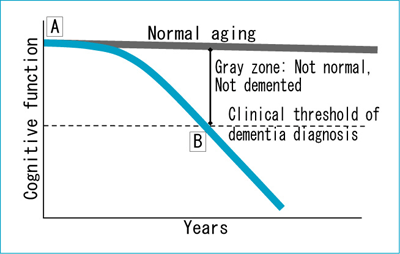 |
| 図 MCIの概念図 |
| 正常から逸脱し,ADを発症した患者さんの経時的な認知機能の変化を模式的に示したもの。現在の診断基準では,いろいろな症状が出揃い生活機能への明らかな影響が及んでからADと診断しているので,診断のポイントを示した点線の位置(Clinical threshold of dementia diagnosis)は下方に来ざるをえない。したがって,正常加齢(上の実線)と認知症との間に大きなgray zoneが生まれることになり,これがmild cognitive impairmentの概念を生み出している。 |
したがって,正常か認知症かの判断は,本来この「傾きの程度」,つまり現在の認知機能を以前のそれと比較することによって可能となるはずである。然るに診断に当たる医師は,発症前の知的機能レベルが個々の患者でどの程度であったか(図の縦軸切片の点Aに相当)についての具体的なデータを持たず,またこの右肩下がり現象の傾斜は個々の患者の知的能力(点Aの高さ)や置かれた環境によって大きく修飾されうることが問題となる。
例えば,現役のエリート役員で常に企業経営に関する重要な判断を求められている方がアルツハイマー病(Alzheimer Disease;以下AD)を発症した場合,さまざまな場面で判断のミスが生じ,「社会生活機能の低下」が周りの目からも明らかで,この傾斜は大きく見え,認知症との判断に結びつきやすいこととなる。一方,息子夫婦と同居し,3度の食事は運ばれ病院通い以外はほとんど外出もしない方では,たとえADを発症してもこの傾斜は緩やかにしか見えず,「漢字はもともと書かなかった。趣味らしい趣味もなかった」となると認知症かどうかという判断はより困難となる。
正常と異常の間=MCI
より操作的な米国のADの臨床診断基準であるNINCDS-ADRDAやDSM-IVでも,「記憶障害のみならず,失語・失行・実行機能障害なども見られ,複数の脳領域にまたがって高次機能が障害された結果として,以前の日常生活機能レベルからダウンし自立した生活が維持できない」ことが確認されて初めて認知症と診断されることになっている。しかし,図の点線でclinical threshold of dementia diagnosisと示した横線をどこに引くかについてはまったくの臨床的判断であり,決して客観的とは言えない。したがって,縦軸切片(点A)と横線上の点Bとの間の中間的なグレイゾーンに位置するようなケース,つまり正常とも言い難いが,しかし認知症の診断基準を満たしているわけではない一群の患者を認めざるを得なくなる。実際,(1)記憶障害は明らかであるが,その他の認知機能は正常で日常生活に大きな影響が及んでいない場合,あるいは(2)軽度の記銘力低下,言語機能低下,視空間機能低下,注意分割機能低下など複数の高次機能障害があるが,その総和としての機能低下が認知症といえるレベルにまで達していない場合は,操作診断上は認知症とはならないことになる。これが,MCI(Mild cognitive impairment;軽度認知機能障害)である。つまり,MCIとは,正常でもないし認知症でもない状態を指すのである。
MCI概念の変遷
このグレイゾーンに対して,主としてヨーロッパの研究者はAge-associated memory impairmentやAging-associated cognitive declineなどと呼び,正常加齢現象の行きつく先として認知機能低下が(ある程度は)起こりうると考えてきた(Normality model)。これに対してPetersenらをはじめとする米国グループは,MCIという概念を提唱し,正常加齢のみでは神経細胞数は減少せず(したがって,認知機能は低下せず),認知機能低下は病的状態に基づくと考えた(Pathology model)。MCIは表面的には軽症であっても,疾患そのものは進行性で,将来認知症へと重症化する可能性のある前駆段階と考えられている。1999年,シカゴにて世界各国からAD研究者が一同に集まり,MCIについての集中的な討論を行った。その結果,MCIを1つのclinical entityとして表現することは現時点では困難であり,表現型から以下のような3つのsubtypeに分類することとなった。即ち(1)Amnestic type:健忘型,(2)Multiple cognitive domains slightly impaired type:複数の高次機能領域にまたがって極軽微な障害があるが,全体としては認知症といえる程重症ではないタイプ,(3)Single non-memory domain impaired type:記銘力以外の高次機能領域,例えば言語,視空間機能などで明らかな障害があるタイプである。
この中で,amnestic typeが1995年以来言われているMCIに相当し,表(左)のような操作的診断基準が提案されている。この中で,「年齢や教育レベルの影響のみでは説明できない記憶障害が存在する」ことを客観的に示すことが最も重要な点であるが,どのようなバッテリーを使うのか,あるいは正常高齢者との境界をどのように設定すべきなのかについてのこれ以上の提案はなされなかった。
ヨーロッパと米国のこのような長年の議論を踏まえ,2003年9月スウェーデンのWinbladらは,コンセンサス会議と銘打ってMCI Key symposiumを開催した。この会議では,これまでのヨーロッパ学派と米国学派の主張の両者をうまく取り入れ,表(右)のように,玉虫色にまとめられた。
| ||
| 表 MCIの臨床的・病因論的多様性 | ||
| 1999年のPetersenらの診断基準と2003年のWinbladらの診断基準の比較。この2つの会議を経て,MCIは単なるADの前駆状態ではなく,臨床的にも病因論的にも多様であることが認識されていったが,各国の研究者が認知症の前段階に目を向け認知症の早期診断・早期治療が議論されるようになった意義は大きい。 |
その骨子は,(1)MCIは正常でもなく,DSM-IVやICD-10で記載されているところの認知症症候群でもない。つまり図において正常と認知症の中間ゾーン(点Aと点Bの間)に相当する。(2)以前に比して認知機能の低下があるが,日常生活機能は自立あるいは軽度の障害を認める程度に留まる。(3)臨床的多様性として,amnestic type,multiple domain type,single non‐memory typeを認める一方で,背景疾患として変性疾患,血管障害,薬物・代謝異常,外傷性,精神科疾患など病因論的にも多様であるというものである。
この中で注目すべきことは,認知機能の右肩下がりの状態,つまりdecline=低下が重要であって,declineの結果必ずしも障害のレベルにまで達している必要はないという判断である(つまり神経心理テスト上は正常範囲でもよい)。
認知症は生活習慣病か?
すべてではないにしてもMCIがさまざまな認知症の前駆状態を含むとすれば,認知症の予防はMCIへの対策でもありうる。SwedenのGoteborg大学のSkoogらは,70歳時には認知症の認められなかった382名をその後最長15年間追跡し,79-85歳までの間にADを発症した者の70歳時点における高血圧との関連を調査した。その結果,ADを発症した者は,有意に高血圧(収縮期高血圧 p=0.03,拡張期高血圧 p=0.004)の罹患が多いことが明らかとなった。Skoogらは,高血圧はsmall vessel disease(頭蓋内穿通枝動脈)を引き起こし大脳白質病変を形成することで認知症の発症を早めていると推測している。本邦のYaoらも同様に佐賀県背振村住民調査においてMRIを用い高血圧と大脳白質病変との関連を指摘している。
最近,東北大学老年・呼吸器内科のOhruiらは,過去に東北大学病院で高血圧治療を受けた4124人の高血圧患者を調査し服用薬とAD発症との関連を検討した。その結果,約8年の間に105名の患者がADの診断を受けた。脳血液関門を通過し脳に移行するアンギオテンシン変換酵素阻害薬(ACE阻害薬,n=437)を服用している患者は,脳移行しないACE阻害薬(n=997)を服用している患者に比してADの発症が4分の1に抑えられたという驚くべき結果を報告した。
Rotterdam研究では,糖尿病患者692名を含む6370名の地域住民を平均2年追跡した結果,AD89名を含む126名の認知症患者が同定された。糖尿病であることは,耐糖能正常者に比してVaD(脳血管性認知症)のみならず,ADの発症リスクも上げていることが示され,特にInsulin治療を受けている糖尿病患者では,AD発症のリスクは約4倍上昇していた。
糖尿病は,糖質の利用障害が中核である疾患であるが,神経細胞が糖の利用障害に陥った結果,神経細胞死がもたらされADを発症すると考える研究者もいる。2000年Wolozinらは,ロバスタチンやプラバスタチンを服用している高脂血症患者からのADの発症が有意に低いことを報告した。また,Refeloらは,ADの遺伝子改変マウスモデルにおいて,高コレステロール食の負荷はアミロイド蛋白の蓄積を促進させることを報告し,スタチンによる高コレステロール血症治療の理論的根拠となった。
Abbottらは,運動可能な71-93歳のハワイ在住の日系アメリカ人男性2257名を対象として,1日当たりの運動距離と5年後の認知症発症の関連を調査した。追跡期間中に158名の認知症患者が確認された。年齢補正後も,歩行最小群(1日当たり0.4km未満)では,1日当たり3.2km超群に比して約1.8倍認知症の発症リスクが高かったことを報告し,活発な生活習慣の促進が認知機能の維持に有効である可能性を示唆した。
Ruitenbergらは,アルコールと認知症の関連を疫学調査で明らかにした。認知症でない地域在住の55歳以上の住民5395名を平均6年間追跡し,197名の認知症患者を同定した。認知症の内訳は,AD146名,VaD29名,その他22名であった。まったくアルコールを飲用しない人に比して軽度から中等度(1-3杯)のアルコールを飲用する人は相対危険度は0.6(95%CI:0.38-0.90)と有意に低下していた。また,この認知症抑制効果は,アルコールの種類に依存しなかった。
