| 連載 第20回 |
再生医学・医療のフロントライン | ||||||
間葉系幹細胞
| |||||||
間葉系幹細胞の可塑性
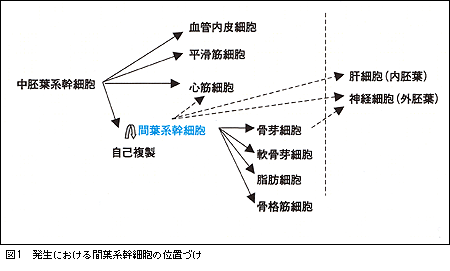
 再生医療・再生医学は次世代医療の柱として脚光を浴び,現実のものとなりつつある。現在,その治療戦略の中心に位置するのが幹細胞システムの利用である。発生の段階から老年に至るまで,生体にはさまざまなステージの幹細胞が存在している。すべての細胞に分化しうる全能性幹細胞を出発点とし,次第に分化方向を運命づけられていく前駆細胞群の中で,どの細胞を用い,その細胞をどのようにコントロールしていくかが今後の臨床応用への大きな鍵となる。間葉系幹細胞は骨,軟骨,脂肪,筋に分化が可能な細胞として認識されていたが,実は驚くほど可塑性を持っていることが明らかにされつつあり,心筋,神経,皮膚,肝臓など胚を越えた分化が示されている。この細胞は間葉系組織のある組織すべてに存在すると考えられているが,最も採取が容易で培養技術の確立しているのが骨髄間葉系幹細胞である。
再生医療・再生医学は次世代医療の柱として脚光を浴び,現実のものとなりつつある。現在,その治療戦略の中心に位置するのが幹細胞システムの利用である。発生の段階から老年に至るまで,生体にはさまざまなステージの幹細胞が存在している。すべての細胞に分化しうる全能性幹細胞を出発点とし,次第に分化方向を運命づけられていく前駆細胞群の中で,どの細胞を用い,その細胞をどのようにコントロールしていくかが今後の臨床応用への大きな鍵となる。間葉系幹細胞は骨,軟骨,脂肪,筋に分化が可能な細胞として認識されていたが,実は驚くほど可塑性を持っていることが明らかにされつつあり,心筋,神経,皮膚,肝臓など胚を越えた分化が示されている。この細胞は間葉系組織のある組織すべてに存在すると考えられているが,最も採取が容易で培養技術の確立しているのが骨髄間葉系幹細胞である。
骨髄は造血の主要臓器であり,含まれる細胞の中心は造血細胞である。これらの細胞を支持するものの1つとして間質細胞が存在する。間質細胞は造血を維持するために網状構造をとり,直接ないしは間接的に血液細胞の分化をサポートしている。この骨髄間質細胞の中に多分化能を持つ間葉系幹細胞が含まれている。
骨髄間質細胞中からの幹細胞の分離
骨髄液を採取し培養皿に付着した骨髄間質細胞は均一な集団ではなく,分化段階の異なる細胞の集合体である。この中で多分化能を持つ細胞のみを選択することが可能であれば,さまざまな臓器再生の強力な細胞源となる。幹細胞の選別を可能とするためには細胞表面抗原発現の違いを利用するのが有望な手段と考えられる。しかし特異的なマーカーは現時点では明らかではなく,いくつかのマーカーの組み合わせで選別しているのが現状である。私たちはマウス骨髄由来間葉系幹細胞株を樹立し表面抗原による未分化マーカーの探索を行なっている。セルソーターを用いた検討より現在はCD34+,CD117(c-kit)+,Sca-1+が未分化の指標と考えている。ヒト骨髄細胞においてはSH-2(CD73),SH-3(CD105),STRO-1,CD13,CD45などが有力な未分化マーカーとして報告されているが,いまだコンセンサスは得られておらず,今後のさらなる解析が待たれる。細胞寿命延長による細胞数の確保
試験管内・小動物において,間葉系幹細胞が多分化能を持つことは証明された。しかし臨床に用いるためには莫大な数の細胞が必要となる。現在の培養技術では採取した初期細胞の増殖には限りがあり,人体の欠損を修復するには不十分と考えられる。これに対応する戦略の1つとして細胞自身の寿命を延長し用いることが試みられている。細胞寿命のメカニズムにテロメア遺伝子の短縮が関与しているが,このテロメアの修復を行なう酵素テロメレースの活性を上げる因子の遺伝子を細胞に導入することで大量に細胞を増殖することが可能である。私たちの研究室においても,数種類の遺伝子を導入したヒト骨髄間質細胞を用いており,多分化能が維持されていることは確認している。この多数回の分裂を重ねた細胞が果たしてどこまで分化能を維持していくのか,また染色体異常を生じてこないのかを今後詳細に検討する必要がある。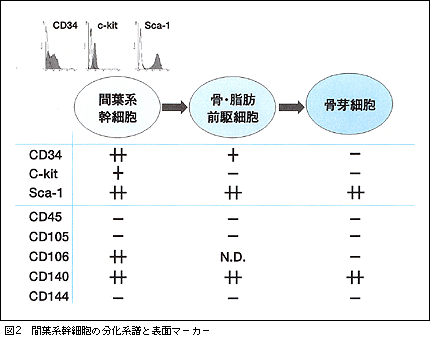
将来的展望
間葉系幹細胞に関する研究は日々進歩しており,その可塑性が明らかになるたびに再生医療への夢が膨らむ。しかし,その一方でこの細胞を用いた現実的な“モノ”ができていないのも事実である。分化可能な細胞の単離・分化誘導法の確立,遺伝子導入による細胞量の確保のみならず,骨や軟骨などの形を要求される組織作りには細胞の足場(培養担体)が必要である。足場に成長因子などを複合化することで細胞増殖や分化誘導をコントロールすることも可能であり,工学的手法が幹細胞生物学に新たな展開をもたらすことが期待される。
