| 連載 第14回 | 再生医学・医療のフロントライン | ||
網膜の機能再生
| |||
神経幹細胞から網膜細胞へ
 成体哺乳類の中枢神経の中で常に神経再生が起こっていることが判明し,その源となる神経幹細胞を未分化状態で培養増殖させることが可能となったことは,中枢神経疾患の細胞移植治療に希望を与えた。網膜疾患については1980年代の動物実験の後,1990年半ばからヒト胎児網膜の細胞移植が行なわれているが,胎児網膜を使用することによる倫理的,および量的問題を解決するものとして神経幹細胞が期待されている。
成体哺乳類の中枢神経の中で常に神経再生が起こっていることが判明し,その源となる神経幹細胞を未分化状態で培養増殖させることが可能となったことは,中枢神経疾患の細胞移植治療に希望を与えた。網膜疾患については1980年代の動物実験の後,1990年半ばからヒト胎児網膜の細胞移植が行なわれているが,胎児網膜を使用することによる倫理的,および量的問題を解決するものとして神経幹細胞が期待されている。
1996年にわれわれは成体ラット海馬由来神経幹細胞の網膜移植における高い生着と神経分化率を観察し,神経幹細胞の網膜移植細胞源としての可能性を示した。
その後,幹細胞網膜移植についてわかってきたことは,脳(海馬)由来の神経幹細胞は移植によって網膜内に生着し神経に分化するものの,網膜神経細胞に完全に分化するのは難しいということである。一方,眼球由来の神経幹(前駆)細胞,例えば毛様体由来網膜幹細胞は培養により各種網膜神経細胞に分化する。また,虹彩細胞は視細胞分化に必要なホメオボックス遺伝子Crxを導入することによって視細胞特有の蛋白ロドプシンを発現する細胞に分化する。脳由来の神経幹細胞では同様にホメオボックス遺伝子Crxを導入してもロドプシン陽性とならなかった。他に網膜固有の細胞に分化することが判明しているのは,現時点では胎児網膜由来神経幹(前駆)細胞とES細胞のみである。
臨床までの距離
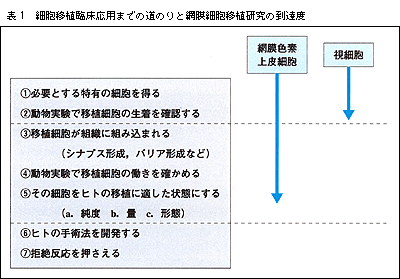
臨床までの距離は,網膜細胞の種類によって異なる。また,どの程度の効果を求めるかによっても違ってくる。胎児網膜細胞移植のように効果がはっきりしない状態で安全性を問うレベルであれば,すでに臨床に達していると言える。視力を正常に回復するという効果を求めるならば,それは遠い未来であると言わざるを得ない。ここではわずかでも効果を認める可能性を持った臨床治療となるまでの距離と仮定する。網膜細胞移植の臨床応用までの道のりを考えると表1のようになる。
加齢黄斑変性などで障害される網膜色素上皮細胞は,貪色作用を持つ特殊な網膜細胞であり,神経細胞ではなく上皮様の性質を持つ。網膜色素上皮細胞移植ではシナプスを形成する必要はないので,貪色作用,物質輸送や網膜血管バリアとしての働きなどを持つ細胞を挿入し,それがうまく生着すれば移植治療となる。貪色作用を持つ色素上皮細胞はヒト胎児網膜色素上皮細胞,本人の虹彩色素上皮細胞,ES細胞由来網膜色素上皮細胞(現在はサル)と候補は揃っており,働きも確認済みなので表1の(1)(2)(3)(4)はクリアされており,(5)の途中である。細胞の移植法(6)は改良を加えるだけなので,拒絶反応の問題(7)をクリアすれば臨床応用可能と思われる。
一方,網膜色素変性や網膜剥離などで障害される網膜視細胞は,光を受容する特殊な神経細胞である。ヒト胎児網膜細胞移植によって拒絶反応が少ないことは判明しているが,視細胞を大量に得ることが難しい。何とか(1)の特有の細胞を得ることはでき,(2)の生着までは達成されたが,(3)のシナプスを形成するという保証は未だなく,(4)正しい働きをするためには視細胞の方向性も問題となってくる。つまり(1)(2)がクリアされただけで,これから難しい部分である(3)(4)(5)が残っている。移植が効果を示すためにはまだ遠いと言える。ただし,そこまで来れば(6)(7)は容易である。
今後の方向性
網膜色素上皮細胞移植は,細胞シートの開発と移植法の改良(すでに移植法はあるので)が今後の課題であろう。視細胞移植に関しては当面のゴールは失明状態の目に光を感じさせる(視細胞が何らかの細胞とシナプスを形成し,とにかく光刺激を中枢まで神経信号として伝える)ということと考えている。視細胞の配列方向や正しいシナプス形成,つまり視機能の向上はその後の問題である。さらに,神経幹細胞の移植にはドラッグデリバリー的効果もあり,視細胞の変性を遅延させるなどの効果は,容易に達成されるかもしれない。
