〔連載〕How to make
クリニカル・エビデンス
-その仮説をいかに証明するか?-
浦島充佳(東京慈恵会医科大学 臨床研究開発室)〔第23回〕ストップ・ザ・狂牛病(7)
観察バイアスの可能性
疫学は,病気の原因をマクロ的アプローチにより見つける学問と言っても過言ではないでしょう。ですから,原因と結果,この場合,「牛肉摂取」と「変異型クロイツフェルト・ヤコブ病(vCJD)の発生」をまず個々に評価するわけですが,その際にバイアスを含有するかもしれません。例えば,vCJDの患者さんのいる家族に,患者さんの食生活をインタビューすれば,牛肉摂取が誇張されるかもしれません。また,vCJDの診断も難しいでしょう。海外では確定診断のために生存中に脳の生検を行ないます。しかし,きわめてvCJDの疑いが強い臨床症状を呈した場合に限られます。日本では,生存中に脳の生検は行なわないので,診断率は下がるでしょう。また,今でこそ若年者で急速に精神症状,痴呆をきたせば積極的検査を行なうでしょうが,老人であったり,症状が軽い場合は,vCJDであっても診断されないかもしれません。
さらに,vCJDの臨床症状が認められなくても病理検査をすると,異常プリオンがプラークを形成している,あるいは病理検査では正常でも,感度のよい分子生物学的検査で異常プリオンが検出できるかもしれません。ひょっとすると,潜在型vCJDはもっと広い範囲に蔓延しているかもしれないのです。よって,「vCJDの発生頻度は万が一よりも少ないから安全です」という理論は重症例だけに当てはまることかもしれないのです。
変異型クロイツフェルト・ヤコブ病の第1例目は1994年でよいのか?
そもそもこの10人の報告は,「イギリスで狂牛病が増え,クロイツフェルト・ヤコブ病(CJD)も並行して増えているのではないか?」という疑問に答えるべくして,1990年より行なわれた全国調査に端を発します。しかし,それより前にvCJD発生は本当になかったのでしょうか?パプアニューギニアで発見されたクールーは,少なくともプラーク周辺の空胞形成の多寡を除いて病理組織学的に類似しています。ただ,vCJDのプリオン遺伝子多型がメチオニン型であるのに対して,クールーの遺伝子多型はヴァリン型である点が異なります。両疾患の異常プリオンをウエスタンブロット(蛋白を解析する方法)で比較した論文は見当たりませんでした。
つまり,vCJDが狂牛病とクールーのどちらにより近いのかは示されていないのです。そして,カリバニズムという風習がなくなった今も,クールーの発生はなくなっていない点も気になります。また,クロイツフェルトが1920年に報告した最初の症例は23歳で死亡しており,その病理組織はvCJDに類似しています。もしも,vCJDが狂牛病発生以前から存在したとすると,少なくとも狂牛病ではvCJD発症のすべてを説明できないことになります。
潜伏期と伝播期の相違
感染症と伝染病はほとんど同義ですが,感染症とは微生物を軸に,伝染病とは人を軸に考える点で異なります。通常,感染症では微生物が体内に侵入し,これが増殖し一定の限界を超えると臨床症状を呈するようになります。その間を潜伏期と呼びます。しかし,人を軸にとった時,「うつるか否か」が最大の関心事なのです。健康保菌者のように発病しないが,他者への感染性だけを持つキャリアも伝染病を考える際には重要です。よって,狂牛病が異常プリオンを体内に取り込み,いつから人に伝播性を有するようになるのかが争点となります。理論上症状を呈していなくとも,異常プリオンの溜まった組織を摂取すれば伝染する可能性はあるからです。日本の農水省は最初,狂牛病検査対象を30か月以上としました。イギリス行政を真似してのことです。しかし,現時点ではいつから人への伝播性を示すのかまったくくわかっていないのが現状であり,すべての牛に関して検討するべきです。
異常プリオンを伝播するリスク臓器
羊スクレイピーやvCJDでは,異常プリオンは脳で蓄積する前,扁桃腺,腸管パイエル板,リンパ節,脾臓などのリンパ組織あるいは血液に出現します。よって,経口的に摂取された異常プリオンは,腸管からリンパ組織に受け渡され,末梢神経,脊髄,そして脳へと伝播すると考えられています。類似の現象は,マウスやサルで認められていますが,なぜか肝心の狂牛病では確認されていません。しかし,肉骨粉中の異常プリオンが何らかの末梢経路を経て牛の脳に移動することは確かなわけで,脳に異常プリオンが認められなかったからと言って,その牛由来の肉や製品が絶対に安全とは言えないのです。事実,vCJD患者の脾臓あるいは扁桃腺をマウス脳に注入すると病変をつくります(Lancet 2001; 358: 208-9)。つまり,感染性があるのは脳組織だけではないことを示しています。また,検査で異常プリオンを検出できる感度に達する前に伝播力を示すこともあり得る点も,この研究結果は示しているのです。CJDはかつてスローウイルス感染症と呼ばれていました。しかし,フォルマリン処理しても熱処理しても感染性を失わないことから,感染性蛋白,プリオンの発見につながったのです。異常プリオンは600度の高熱でも失活しないとの報告もあります(PNAS 2000; 97: 3418-21)。このことが何を意味するか読者の皆さんはわかりますか?
オートクレーブで処理をした手術器具に付着したプリオンが次の手術患者さんに感染し得ることを意味するのです。また,現在43万トンの肉骨粉がイギリスで貯蔵され,850度以上で燃やしたり,バクテリアに食べさせたりしていますが,これらを完全に使い切るまでには時間がかかり,非常に危険なことなのです。異常プリオンが土壌や飲み水に混入したらどうなるのでしょうか?
今のところ,ワクチンからのvCJDは報告されていませんが,かつて牛の組織を使用していたため心配されます。
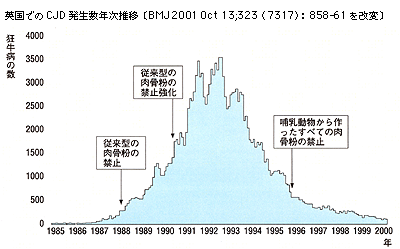
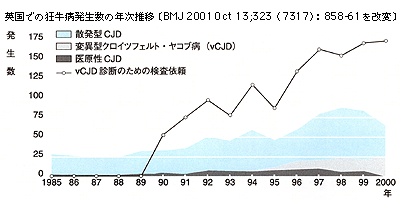
そして,イギリスでは狂牛病の発症ピークから約10年経っているので,潜伏期が十数年だとすれば,vCJDはそろそろ急増するはずですが,今のところ急増の兆しはありません。この先10年,急増,そして減少しなければ,狂牛病以外の伝播経路も考えなくてはならないでしょう。いずれにしても,まだまだ予断を許さない状態なのです。
(この項つづく)
