| 連載 第12回 | 再生医学・医療のフロントライン | ||
血液の再生-造血幹細胞の体外増幅
| |||
 造血幹細胞は骨髄のみでなく,末梢血や臍帯血にも存在し,それぞれに特徴のある造血幹細胞の供給源として注目されている。再生医学研究の血液分野で現在,もっとも注目されているのは造血幹細胞の体外増幅である。この技術の進歩は,移植後の生着の促進,ドナーの負担の軽減,医療資源の効率的活用などの現実的なメリットばかりでなく,遺伝子治療や血液の人工大量生産など将来の医療に大きなインパクト与えるものとして期待されている。
造血幹細胞は骨髄のみでなく,末梢血や臍帯血にも存在し,それぞれに特徴のある造血幹細胞の供給源として注目されている。再生医学研究の血液分野で現在,もっとも注目されているのは造血幹細胞の体外増幅である。この技術の進歩は,移植後の生着の促進,ドナーの負担の軽減,医療資源の効率的活用などの現実的なメリットばかりでなく,遺伝子治療や血液の人工大量生産など将来の医療に大きなインパクト与えるものとして期待されている。
造血幹細胞の体外増幅システム
筆者らはマウス骨髄ストローマ細胞をfeeder layerとして利用した膜分離型共培養系を造血幹細胞の体外増幅システムを開発した。この培養系は径0.45μmの小孔を多数持つフィルターの下面裏側にマウス骨髄ストローマ細胞(HESS-5)を付着させ,フィルター裏面を覆うように形成させた単細胞層に1.5GyのX線照射を行なって増殖能をなくした後,フィルターの上面表側に臍帯血から分離したCD34陽性細胞を播種し,トロンボポエチン(TPO),FL-2,幹細胞増殖因子(SCF)の存在下で無血清培養を行なうものである(図1)。これによって,CD34陽性細胞はフィルターの小孔から伸びた下面のHESS-5細胞の一部と直接の接触が可能となる一方,細胞同士は隔てられているので,培養したCD34陽性細胞だけを純粋に回収することができる(図2)。5日間の培養後に回収された細胞数は約17倍,CD34陽性細胞として約5倍,その中でもより未分化な前駆細胞を含むCD34陽性CD38陰性細胞は110倍に増えた。また顆粒球,赤芽球,マクロファージ,巨核球を含むコロニーを形成する多分化能前駆細胞(CFU-GEMM)は約11倍に増幅された。さらにヒト骨髄ストローマ細胞上で5週間培養した後にも造血コロニーを形成する能力を持つ長期培養開始細胞(long-term culture-initiating cell, LTC-IC)は約25倍に増幅した。
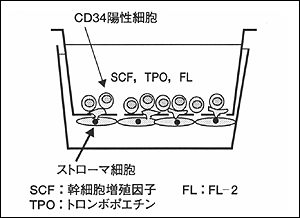 図1 ストローマ細胞を用いた造血幹細胞の膜分離型培養系 |
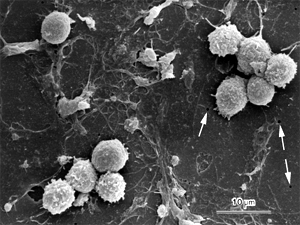 図2 膜分離型培養系で培養中の細胞の走査電顕像。CD34陽性細胞は膜の微細孔を通して進展したストローマ細胞の細胞質と接触しながら増殖している。矢印は径0.45μmの小孔を示す |
すべての血球系列に分化可能な多能性幹細胞を含む細胞系
筆者らの培養系で体外増幅した臍帯血CD34陽性細胞を,重症免疫不全のためにヒトの細胞を拒絶できない遺伝マウス(NOD/SCIDマウス)に移植して7週後のマウス骨髄におけるヒト由来細胞の造血能を観察するSRC assay(SCID mouse repopulating cell assay)で,50%以上の骨髄細胞がヒト型となっていた。一方,培養前のCD34陽性細胞ではわずかに約4%がヒト型細胞であったことから,SRCのレベルでも確実に増幅が可能であることが判明した。多数のNOD/SCIDマウスを用いた定量実験では,培養後のSRCの増幅は10-12倍であり,これまでの短期培養系では最も高い増幅効率を得た。またNOD/SCIDマウス骨髄を再構築したヒトCD45陽性細胞は,同時に顆粒球に特異的なCD33陽性細胞を21.9%,単球・マクロファージに特異的なCD14陽性細胞を5.6%,赤芽球に特異的なグリコフォリンA(Gly A)陽性細胞を4.1%,巨核球に特異的なCD41陽性細胞を7.7%,Bリンパ球に特異的なCD19陽性細胞を6.4%に含むことから,多分化能を有することが証明された。さらにこの再構築ヒトCD45陽性細胞は,CD34陽性細胞を5.4%含んでいた。これらの特徴は,多分化能と自己複製能を合わせ持つという幹細胞に特有の性質を示している。
これまで,NOD/SCIDマウスを用いた多分化能解析で培養CD34陽性細胞からT細胞への分化を確認できなかったが,最近開発されたIL-2受容体のcommon γ鎖遺伝子をノックアウトしたNOGマウスを用いることにより,T細胞への分化を確認した。また樹状細胞への分化をも確認した。したがって,われわれの開発した培養系での体外増幅幹細胞は,生理的に存在するすべての血球系列に分化可能な多能性幹細胞を含むことが示された。
臍帯血は骨髄,末梢血に次ぐ新たな造血幹細胞の供給源として期待されている。臍帯血は採取に際してドナーの負担がなく,移植後の移植片対宿主反応(GVH)が比較的弱いため,組織適合抗原(HLA)が2抗原不一致でも移植が可能であるなどの利点がある一方,採取細胞数が限られているために対象は小児が中心で,ほとんどの成人には細胞数が不足している。また骨髄移植や末梢血幹細胞移植に比して生着や免疫能の再構築が遅いことが問題である。臍帯血移植を安全かつ有効に行なうとともに,臍帯血移植を成人にも広く利用できる造血幹細胞の体外増幅システムの臨床応用が期待されている。
異種移植の安全性は?
しかし,筆者らの開発したマウス骨髄ストローマ細胞を利用した体外増幅システムで解決しなければならない最大の問題点は,異種細胞(HESS-5)の安全性の問題であった。本培養系ではHESS-5細胞がCD34陽性細胞に混入しないことは高感度PCR法によって確認しているが,細胞の破片やウイルスがフィルターを介して混入する可能性は否定できない。最近わが国において細胞および組織を用いた医薬品および医療材料に関する指針が出されたが,どこまで確認すればよいかは必ずしも明確でない。また,プロセッシングした細胞や組織の安全性を検査するシステムはまだ整備されていない。筆者らは自ら参加した厚生科学研究「組織細胞工学技術を用いた医療材料・用具の有効性,安全性,品質評価方法に関する研究」班(主任研究者=国立衛生試験所 中村晃忠)の総括研究報告書(1999)や,1998年に米国食品医薬品局(FDA)が提出した「体細胞療法および遺伝子治療のガイダンス」の勧告に準拠して11項目についてHESS-5細胞の安全性の検査を,米国BioRelianceSM社(国内代理店=加商,東京)に依頼して実施した。そしてこれらのすべての検査項目について異常なしの報告を受けた。また臨床応用のための作業手順書を作成し,独立した作業環境および専任技術者の確保を行なった。
難治性血液疾患への幹細胞移植
このような状況を踏まえて,われわれは難治性血液疾患を対象とした体外増幅臍帯血幹細胞移植の安全性と有効性を検証するための臨床第I/II相試験を計画した。対象は臍帯血移植の適応のある患者で,血縁者および骨髄バンクに適合ドナーがないか,あっても待機できない状態にある患者とした。臍帯血有核細胞は1.7-3.0×107個/kgにあるものを選択し,そのうち1.0×107個/kgはintactのままとし,残りの有核細胞からCD34陽性細胞を分離して体外増幅のための培養を開始する。Intactの細胞とCD34陰性細胞は開始日に通常の造血幹細胞と同様に移植する。CD34陽性細胞はHESS-5細胞を利用した膜分離型共培養法で短期無血清培養し,5日後に回収して追加移植するものとした。臨床試験実施計画書は東海大学医学部倫理委員会の承認を得て,適格症例を待機中である。異種移植をめぐる最近の動向
一方,本培養系では膜を介してではあるが,ヒト細胞がマウスストローマ細胞と接触する。従来,「異種移植」とは「ヒト以外の動物に由来する生きた細胞・組織・臓器を,ヒトに移植,移入又は体外灌流に用いること」と定義づけられてきた(第26回厚生科学審議会先端医療技術評価部会議事録,2000年9月22日)。このことからわれわれの方法は異種移植には当たらず,2000年12月に厚生省(当時)医薬安全局から提示された薬事法による「細胞・組織利用医薬品の取り扱い及び使用に関する基本的考え方」に基づいてヒトや動物の細胞・組織を用いた医薬品・医療用具の開発において,細胞・組織に由来する感染症伝播の危険性,培養細胞の製造工程中におけるがん化等の品質および安全性を確保した上で,人権の保護などを確保しつつ臨床応用に向かうこととした。しかし,2002年3月8日に米国のFDAの通知として「生きた動物細胞,組織又は臓器と体外で接触した細胞をヒトに移植する」場合も異種移植として米国厚生省のPublic Health Service(公衆衛生局,PHS)によるPHSガイドライン「異種移植の感染症問題に関する指針」(2001年1月29日)に準拠することを求めた。つい最近,7月9日に厚労省医政局課長通知で同様の方向が持ち出された。
このような背景から,われわれの開発した培養系もその規制の下に行なわなければならない趨勢にあると理解する。また最近,厚生科学審議会において「ヒト幹細胞を用いた臨床研究のあり方に関する専門委員会」(委員長=京大中畑龍俊)において検討が開始されており,この方面におけるわが国の指針が整理される方向にある。
今後は,本培養法の安全性確保のみならず,ストローマ細胞の造血支持能を含む分画を用いた培養法,さらに造血幹細胞自己複製分子の同定と遺伝子クローニングなどの研究を進める予定である。
