<インタビュー>
再生医療の実用化はどこまできたか?
上田 実氏(名古屋大学大学院教授・頭頸部感覚器外科学)
幹細胞やヒトES細胞の研究が進む中で,再生医療という新しい治療が現実のものとなり,すでに培養皮膚などは臨床応用の段階まで進んでいる。近いうちに大学病院,そして一般開業医が当たり前のように再生医療を患者に行なう日がくるのだろうか。
上田実氏(名古屋大学大学院医学系研究科教授)はイヌにおいて完全な歯の再生に成功し,すでに培養皮膚,歯槽骨の分野ではその技術を企業に移転,一般開業医でも利用できる「製品」として生産システムの構築を進めている。
今,再生医療はどこまで実用化されているのか,そして今後一般に普及するには何が必要なのか,氏にインタビューを行なった。
再生医療が求められる背景
――最初に,再生医療の現状についてお聞きしたいと思います。上田 再生医療による臓器の再生は2つの理由から必要とされています。
いわゆる脳死移植法が制定されてから6年経っていますが,日本の移植医療を取り巻く環境整備が遅々として進まないために,まだ脳死からの臓器移植は26例しか行なわれていません。これが理由の1つです。たとえば肝臓移植を例に取ると,アメリカでは年間5000例ぐらい行なわれていますが,日本では数例だと思います。その代わり日本では他の先進国に比べて生体部分肝移植が非常に発達していて,これは臓器が手に入らないことによって発展した外科手技といえるでしょう。しかし,健康なドナーの体に傷をつけなければいけないという問題があります。
一方,日本は人工臓器の研究が伝統的に進んでいたのですが,この分野も過去10年くらい大きな発展がなく,性能的な面で臨床応用に近づけていません。これがもう1つの理由です。
こうした理由によって重症の臓器不全症に対する治療法が行き詰まっていたところに,臓器移植を行なってきた医師と,人工臓器の研究をやってこられた方々の実績が融合する形で,再生医療という分野が出てきたのだと思います。
つまり,たとえば肝臓の場合,全体または部分的な肝臓移植ではなく,肝機能の最小単位である肝細胞を取り出し,人工臓器で培われてきた材料,あるいは循環系のシステムの中に移植して肝臓の再生をするというような,新しい展開としての再生医療ができあがってきたわけです。
当然,再生医療の最終ゴールは,臓器移植に代わり得るものにしようと皆が努力しているわけですが,たとえば肝臓をまるごとつくるということになると,肝組織ですから細胞が立体構造を形成することが必要ですし,血管や神経もつくらなければいけませんから,これは容易なことではありません。しかし,肝臓という臓器の一部であれば可能なわけです。
現時点で肝臓の幹細胞を大量に増やすことはできていますので,既存の肝臓の中に元気な幹細胞を移植して,臓器ではなく,幹細胞のレベルで肝臓を再生させるということが可能になりつつあります。つまり悪くなった肝臓にいい細胞を注入して,その部分だけを再生させるわけですが,これは動物を使った基礎実験ではすでに成功しています。
同様のことは心臓・循環器系でも可能です。心筋梗塞などで壊死してしまった筋肉組織の一部に間葉系幹細胞を注入することで心筋を再生させる,あるいは体外で培養した心筋を移植するということも,大動物実験で可能になりました。
脳における再生医療は主にパーキンソン病が対象疾患になっています。パーキンソン病というのはドーパミン産生細胞が変性を起こして,ドーパミンを分泌しなくなることによって起こる病気ですから,ドーパミン産生細胞を体外で増やし,脳の中に移植することで治療できるわけです。これも大動物実験では成功しています。ドーパミン産生細胞を,ES細胞から分化させて大量に培養することもできています。
臨床応用への課題
 上田 しかし,こうした臓器再生はすべてが大動物実験,つまり前臨床の段階で止まっています。この理由は倫理的な問題を含めた法的規制と,ES細胞の分化が完全には成功していないために腫瘍化する可能性があるということです。これが臨床試験への大きな壁となっているわけですが,やがては乗り越えられていくでしょう。
上田 しかし,こうした臓器再生はすべてが大動物実験,つまり前臨床の段階で止まっています。この理由は倫理的な問題を含めた法的規制と,ES細胞の分化が完全には成功していないために腫瘍化する可能性があるということです。これが臨床試験への大きな壁となっているわけですが,やがては乗り越えられていくでしょう。
その一方で,再生医療の中でかなり進歩していて,臨床に堂々と入ってきている分野があります。それは臓器ではなく,組織レベルでの再生医療です。代表的なものは皮膚ですが,これは1980年代に,すでに基盤的な技術が完成していて,アメリカでは推定10万人以上の患者さんが救命されたと言われています。この組織の再生医療という分野は最近になって急速に進歩してきて,骨,軟骨,末梢神経,角膜,網膜といった組織において研究がかなり進んできています。
臓器と組織,この2つの再生医療の進歩の違いは,幹細胞の入手しやすさが影響しています。肝臓の幹細胞に代表される体性幹細胞は大量には手に入りにくいため,ES細胞を使わなければいけません。しかし,幹細胞を容易に採取できる組織,つまり骨,皮膚,角膜,網膜,神経といった組織は,もはや臨床の段階に入っていると言っていいと思います。
これらは自家移植,つまり患者本人の細胞を使っているので免疫抑制剤の必要がなく,臨床的な効果も大きい。技術的にも法的にもハードルが低いので,今後さらに発展していくでしょう。
■“骨を制するものが歯科を制する”
 ――上田先生のところで臨床応用されている研究にはどのようなものがありますか?
――上田先生のところで臨床応用されている研究にはどのようなものがありますか?
上田 私たちのところでは,皮膚,尿管,心臓弁,血管,腱,骨,軟骨,歯肉,粘膜,網膜,角膜,そして歯と,非常に多くの組織と臓器の再生研究を行なっています。このうち歯だけは少し別格ですので後でお話ししますが,それ以外のものは単一の細胞からなる組織という特徴を持っています。つまり,骨は骨の細胞,皮膚は皮膚の細胞だけでできるわけです。
軟骨,骨,皮膚,角膜,神経はすでに臨床応用を行なっており,特に皮膚は140例以上を臨床応用し,対象疾患も火傷,あざ,白斑,瘢痕,褥瘡性潰瘍と多岐にわたっています。3年ぐらい前に日本財団の要請でアフリカでの医療ボランティアに使ったこともあります。現在,培養皮膚はベンチャー企業に技術移転されています。
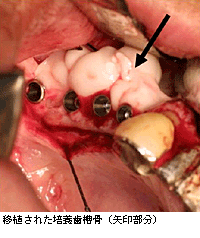
また,骨という組織は歯科の分野では非常に重要で,歯槽膿漏で歯が脱落してしまうと,人工歯根を植立したり入れ歯を施術するためには,顎骨という骨がどうしても必要なのです。したがって,いわば「骨を制するものが歯科を制する」と言ってもよいぐらいに重要な組織なのです。これまではなかなかうまくできなかったのですが,今では骨芽細胞の培養と分化,移植ができるようになりましたので,ほぼ自在に顎骨をつくれるようになっています。
これは歯科の分野から非常に大きな期待を集めています。今年中に臨床応用が100例ほどになる予定で,その後,一般開業医にも普及していくと思います。
培養皮膚の研究が世界的に盛り上がったのが80年代終盤だったとすれば,2000年代には骨の臨床例がドッと出てくると思います。これによって,歯科の分野が大きく発展する可能性が高い。なぜかというと,歯科の分野では先ほど述べたように骨が非常に重要であるということと,歯槽膿漏の患者さんがたくさんいるからです。
そして,その患者さんたちが必要としている再生すべき骨は,それほど大きなものではありません。整形外科が要求するような何百グラムという単位ではなくて,何グラムの単位で歯科の患者さんは救うことができます。そういう長所があるので,骨の再生医療はまず歯科の分野ではじめられて,やがて骨粗鬆症のような大きな骨を必要とする疾患に入っていくのではないかと思っています。
次に血管ですが,たとえば心臓から出るところにある大動脈のような大血管の置換術はこれまで人工血管で行なわれてきたのですが,長期的にみると傷んできてしてしまうという問題があり,より強度の高いものが求められています。私たちは胸部外科との共同研究で,細胞を組み込んだ,おそらく世界でもっとも性能のよい人工血管をつくることに成功しました。これも,臨床応用直前のところにあります。また,腎臓から膀胱につながっている尿管も再生できるようになりました。
このように,単一の細胞でできている組織のうち,皮膚,軟骨,骨,神経,尿管,大血管に関しては,すでに臨床応用がはじまっていますし,これらは「治験」ができる段階にまできています。つまり,これからは研究ではなく臨床だということです。
複数の組織からなる「歯」
 上田 最後に歯の再生ですが,これは今までの話とは違って格段に難しいものです。歯というのは大きいものでも2センチほどですが,外層にエナメル質という人体の中でもっとも硬い組織があります。その内側に象牙質という組織があり,これはだいたい骨の硬さに一致しています。さらにその内側に歯髄というものがあるわけですが,これらが層構造になっていなければいけません。また,噛む力を支えるほど硬いものですから,非常に完成度の高いものでなければ,噛んだときに潰れたり,割れたりしてしまって臨床応用できないわけです。
上田 最後に歯の再生ですが,これは今までの話とは違って格段に難しいものです。歯というのは大きいものでも2センチほどですが,外層にエナメル質という人体の中でもっとも硬い組織があります。その内側に象牙質という組織があり,これはだいたい骨の硬さに一致しています。さらにその内側に歯髄というものがあるわけですが,これらが層構造になっていなければいけません。また,噛む力を支えるほど硬いものですから,非常に完成度の高いものでなければ,噛んだときに潰れたり,割れたりしてしまって臨床応用できないわけです。
また,エナメル質は上皮系,その他の部分は間葉系の幹細胞から分化しているため,起源が違う幹細胞を同時に,しかも層構造になるように培養していかなければいけないという問題もあります。
したがって歯の再生は,体のどこかの部分から1種類の幹細胞を採取して,それを増やして移植するというような単純な戦略では無理なのです。上皮系と間葉系に分かれる前,より上流にある幹細胞を見つけなければいけない。今までの体性幹細胞を使った再生医療とは違ったストラテジーが必要になるわけです。
このために,東京大学の医科学研究所で,歯胚再生学研究部門という,歯の幹細胞の探索を目的とした講座を創設しました。現時点では,その幹細胞の遺伝子解析まではできていませんが,候補となる細胞をいくつか見つけていまして,イヌにおいてその細胞を使って歯の組織の再生に成功しました。これは,人体の発生過程で見られる歯の組織とほとんど同じです。おそらく世界で初めてのデータだと思います。
――具体的にはどのようにして再生させるのでしょうか?
上田 まず,足場となる材料に幹細胞を播種します。この足場材料の形によって前歯や奥歯のように形状が異なる歯をつくることができます。しかし,幹細胞をただ播種すれば歯ができるというものではありません。そのままでは,本来あってはいけない場所にエナメル質や象牙質が形成されるということが起こるので,機械的な振動や,回転させて遠心力をかけるなどの機械的なストレスを加えます。その結果,幹細胞がそれぞれの組織に分化・階層化していくわけですね。例えるなら,粒子の大きさの違う砂を箱に入れて,端にトントン刺激を与えると,ある粒子だけが階層化してくるのに似ています。その刺激の程度と期間の最適な条件はまだわかっていないのですが,ある程度のより分けと階層化には成功しています。幹細胞を移植した段階から完全な歯の形になるまでは,イヌの場合で18-20週です。
これが歯における再生医療研究の,現時点の到達点です。培養時の機械的なストレスが遺伝子レベルでどのように細胞分化に影響を与えるのかは,まだわかりません。こうしたことはサイエンスとしてみると非常におもしろいのですが,私たちが何よりも望んでいるのは,臨床に使える技術です。とにかく,一目散に臨床に使えるところまで持っていくための研究をやって,基礎的なメカニズムの解析は後から解決していこうという姿勢です。いわば,従来の積み上げ型の研究,つまり基礎データによってメカニズムを確認して次のステップへ進むというのではなく,入り口で発見された現象を使って,最終的な段階まで一気に行ってしまおうというわけです。メカニズムは,あとで順次解決していく。このアプローチの仕方は,私たちが患者をみている臨床系の人間だからかもしれません。
――ヒトへの応用は今後どうでしょうか?
上田 おそらく,ヒトでも今のやり方で成功すると思っています。ただ,動物実験であれば入り口から臨床まで一気にできますが,これをヒトでやるわけにはいきません。ですから,まずは動物実験で最終ゴールまで行って,end pointからもう一度戻ってメカニズムを解明する必要があります。それが終わった段階で,歯の再生の全ストーリーが明確になり,ヒトへの臨床に進めるわけです。今はそのためのデータを整理,解析しているところです。
おそらく,2007年,いまから3年くらい先には,初めてヒトの歯での臨床応用が行なわれると思います。歯というのは虫歯で欠けてしまっても,人工材料で補うことができます。同じように,たとえ完全に臼歯や前歯の形にできなかったとしても,歯根の部分さえつくれればいいのです。歯根は間葉系の細胞だけでできていますから,この部分だけを標的とした再生医療は比較的早期にできると思います。しかし,まったくパーフェクトな歯,ということになると,まだ見通しはわかりません。
■「実用化」における3つのカテゴリー
上田 講演などの機会に再生医療の研究発表をしますと,よく実用化についての質問を受けます。たとえば,歯槽骨の再生について,歯医者さんの前で講演しますと,「これは,いつになったら使えるようになりますか」とよく聞かれます。この「いつ使えますか」というのは,実にあいまいな言葉で,「すでに使っています」というのも正解,「もうすぐ使えます」というのも正解,「2007年ぐらいじゃないかと思います」というのも正解なのです。なぜかというと,名古屋大学附属病院の再生歯科外来ではすでに行なっているわけです。しかし,これはまだ実用化したとは言えません。
日本大学や日本歯科大学,東京大学などの大学病院などでしたら,おそらく今年中にできるようになるでしょう。しかし,一般の開業医の先生方ができるようになるという意味でしたら,おそらく2006-07年になるのではないかと思います。
その理由は,こうした再生医療を実用化するには1つずつクリアしなければならない法律があり,その承認を受けるレベルによって,使用できる人といいますか,医療機関が変わってくるわけです。
今,名古屋大学附属病院の再生歯科外来では患者さんを診察して「この人は歯槽骨をつくるべきだ」と判断した場合,まず患者さんに説明をして同意を得ます。そして細胞を採取,約6か月かけて歯槽骨をつくり,それをもとにインプラントや入れ歯が施術されます。ただし,これは医師法の範囲内で実験的にやっている医療です。治療費もいただけませんし,保険適用ではありませんから,私の定義では実用化ということにはなりません。
次に,名大以外の各大学で細胞を培養して,「われわれの責任で,保険適用を受けずに自費でやります」といった場合,これはすぐにでも可能なわけです。しかし,細胞培養の技術を持っている病院というのは,現実にはごくわずかです。ですから,われわれが各病院に技術移転をして,そこで自費診療を受け入れた患者さんに行なうことは可能です。これは薬事法ではなく歯科医師法や医師法の範囲でやることで,患者と医者の合意があればできますし,治療費もいただくことができます。
しかし,これらは一般の歯医者さんにはできません。なぜかというと,細胞培養ができる技術・設備がないからです。仮に技術があって細胞の移植は可能でも,加工と培養は誰かがやらなければいけないわけで,これを企業が担当します。つまり,医師でない方が培養して,それに培養費用を加えて歯科医院などに販売するわけです。これを行なうには,薬事法の適用が必要なので承認を受けなければいけませんが,このハードルがものすごく高いのです。日本は世界一その承認が厳しいので,そこのところでJ-TEC(Japan Tissue Engineering Company)も歯槽骨のオステオジェネシスという会社も止まっているわけです。
ですから,「いつできるか」という質問をされると,この3番目のカテゴリーである一般開業医による利用は2006年か,2007年ということになるでしょう。ですが,大学病院での実用化はできていますし,症例も今年中に100例を超えるでしょう,ということは言えるわけです。
どのようにして再生医療を一般的なものにしていくかというと,やはり薬事法の規制緩和を厚労省に対して求めていくことでしょうね。そして,さまざまな技術的・法的課題について,交渉過程を情報公開しながら,市民あるいは一般社会の目の前でその議論を展開していくべきだと思います。
そうやって規制緩和をしたうえで,その規制を守りながら,承認を受けるための努力をすべきだと思います。具体的な課題はとてもたくさんありますが,われわれは今,そのための努力をしているところです。
再生医療は誰でもできる?
――こうした再生医療の技術移転を受けた企業による,商品としての皮膚や歯槽骨の製造・販売はどのような形態になるのでしょうか?上田 再生医療の王道は,自家の細胞,免疫拒絶を受けない細胞を使って自分の体の一部を治すというものですから,患者自身の細胞を用いた自家移植になります。皮膚を例にあげると,まず医師が患者さんから細胞を採取してJ-TECに送り,そこで培養皮膚がつくられ,もう一度病院に戻すわけです。歯槽骨も同じです。現在J-TECでは,そのシステムを構築中です。
――培養皮膚を利用した治療には,高度な知識や技術を要するのでしょうか?
上田 そんなことはないと思います。
もちろん皮膚移植を行なったことのない人にはできないと思いますが,たとえば脚の皮膚を顔に移植するような皮膚移植ができる人なら大丈夫でしょう。培養皮膚を必要とする方で,皮膚移植の経験がない医師はいないと思います。
ただ,問題は開業している一般の歯科医師が歯槽骨を利用した治療を行なう場合だと思います。一般的に,歯科医師は歯を抜く以外の外科手術を行ないませんから,そういう人たちが細胞移植をするためには,それなりのトレーニングが必要になるかもしれません。
厳しい日本の法的規制
上田 このように,再生医療は技術的には想像以上に進んでいるわけですが,いちばん障壁になっているのは,やはり法的な規制の部分です。日本でのバイオビジネスというのは非常にやりにくい分野で,大きなマーケットとしての可能性があるにもかかわらず,世界一厳しい法的規制のためになかなかうまくいっていないのです。そのため,ほとんどのメディカル・デバイスは輸入品です。こういった状況が,再生医療でも起こる可能性があります。いちばん最初の話に戻りますが,臓器移植はうまくいっていないでしょう? それから,人工臓器もなかなか臨床応用されていませんね。これは主として法律の問題だと私は思います。
また,人工臓器を研究している研究者の能力が海外の研究者に比べて低いかといえば,そんなことは絶対にありません。問題は,つくった人工臓器が製品として使用され,事故が起きた時の補償の大きさ,社会的なバッシングの強さなどだと思います。
ですから,このままでは再生医療においても日本の医療産業,バイオビジネスは,過去の失敗を繰り返すのではないかというのが,私の大きな懸念です。それによって,もちろん産業界も困るわけですが,いちばん困るのは患者さんです。先端医療を自分の国で受けられないわけですから。再生医療は従来のメディカル・デバイスに比べれば非常に大きな可能性がありますから,同じ失敗を繰り返してはならないというのが,私の主張です。
――このままでは技術があっても患者さんに使えない可能性があるわけですね。
上田 そうです。再生医療全体を,まったくニュータイプの人工臓器であり,臓器移植なのだと考えればわかりやすいと思います。プラスティックやシリコンではなく,細胞を材料に使っているだけなのです。
ですから今私は,こうした再生医療技術を日本で利用できるような環境づくりに専念しているわけです。
■企業の支援が普及へのカギ
――企業への技術移転によるメリットというのはどのようなものでしょうか?上田 メリットは非常に大きいですね。さきほど述べた再生医療の普及における3番目のカテゴリーですが,高度先進医療を一般に普及させるためには,絶対に企業の力が必要なのです。
それはなぜか。再生医療を例にとると,一般病院では細胞培養はできません。ただでさえ忙しいうえに,培養技術の習得には時間がかかります。医療従事者でなくてもできることなら,企業の人たちに受け持ってもらえばいいわけです。たとえば心臓弁を病院の工作室のようなところでつくることは不可能でしょう?
ですから,高度医療をやろうとすればするほど,企業の専門家集団の支援が必要なのです。彼らの技術力,生産力,販売力のようなものにどうしても頼らざるを得なくて,結果的には彼らも利益を得るわけですけれども,患者さんも含め皆が得するシステムとして技術移転は必要だと思います。
日本は今までそれをせず,大学の中だけで完結してしまっていました。でも近年になって,ようやく大学発ベンチャーをつくろうという動きがあります。
――すると,新しい技術が一般化していくための土台が作られつつあるわけですね。
上田 そうですね。特に今世紀はバイオの時代だといいますし,生物学系の工学部,理学部や,医学部,歯学部,薬学部,農学部といった,広い意味でのバイオ,生命科学をやっている人たちの技術移転というのが,かつて石油や鉄鋼といった基幹産業にとって代わるだろうというふうに考えられているわけです。その,まさにわれわれがやらなければいけない部分が,これから産業構造の中央にくるわけです。
さらなる発展をめざして
――それでは最後に,今後の研究テーマについてお尋ねします。上田 われわれは今まで単独の組織を研究してきましたが,たとえば「運動器」や「消化器」,「泌尿器」といった診療科別のものを機能させるためには,1か所だけできても仕方がないわけです。たとえば歯だったら,噛む装置全体の中の一部ですから,中枢神経を含めた「咀嚼系」というものがあるわけです。そういった,統合されたコンピュータシステムのような再生系,制御系の研究が必要になってくるのではないでしょうか。そういった研究を,これからしていきたいと思っています。
それから,個別の研究対象としては,重症度の高い,つまり他の方法では治らないようなもので,今まで研究されていなかったようなものをやっていくことになると思います。たとえば網膜ですね。失明の患者さんはかなり多くて,今までの方法では治りませんから,そういったものを研究したいと考えています。
私たちの領域では歯の再生がゴールですから,もちろんそこに重点を置きます。それから,再生医療の実践のための社会システムをつくっていきたいと思っています。今までずっと研究をやってきましたが,臨床応用まで進んだ結果,また新しい課題が見えてきました。2004年の課題としては,それをブレイクスルーしてみたいですね。
――ありがとうございました。(終)
| 上田実氏 名古屋大学大学院医学系研究科頭頸部感覚器外科学講座教授。東京大学医科学研究所教授を併任。東京医科歯科大学歯学部を卒業後,名古屋大学大学院医学研究科を修了。同大学院の助手・講師を経て,イエテボリ大学(スウェーデン),チューリッヒ大学(スイス)留学後,現在に至る。著書に『再生医療とはなにか』(メディア出版),ほか多数。 |
 |
