| 新連載 第1回 | 再生医学・医療のフロントライン |  |
心臓細胞再生の現状と展望福田恵一慶応義塾大学医学部 心臓病先進治療学講師 | ||
再生医学は,全身のあらゆる組織・臓器を対象に,自己の細胞が増殖・分化できる足場となる適切な環境を体内に与えることで,自己の臓器が本来の構造と機能を取り戻すことを目的とした,新しい医療として現在大きな注目を集めている。また,1998年にアメリカで単離されたES細胞(ヒト胚性幹細胞)は,本領域の研究を促進するツールと考えられ,世界に大きなインパクトを与えた。
しかし,急激に研究が発展する中で,臨床応用への可能性が見出される一方,克服すべき問題・課題が明確になってきたのも事実である。
本紙では,すでに2468号(本年1月7日)で特集「再生医学・医療のフロンティア」を企画し,本領域の課題,今後の可能性に関する総論的な話題を提供いただいた。そこでの内容を基礎に,再生医学・医療研究の最先端を,各分野の第一人者にご紹介いただく連載「再生医学・医療のフロントライン」をスタートする。
(編集=京大再生医科学研 清水慶彦氏)
心臓細胞再生をめぐる状況
心臓移植は重症心不全の究極の治療法であるが,世界中の国々でドナー不足が深刻な問題となっている。米国では年間の心臓移植適応症例は7万例とされるが,実際の手術症例は約2000例で,ここ数年横這い状態である。人口が半分の本邦においても,数万例の移植対象患者がいると考えられるが,実際に心臓移植の恩恵を受けるのは年間数例にすぎない。補助人工心臓が限られた期間しか使用できないことを考えると,心臓移植に替わる新たな治療法の開発が必要であることは疑う余地のないところである。これらの問題を解決する手段として,ドナーを必要としない心臓移植,すなわち再生心筋細胞の移植による新たな治療法の開発が待ち望まれていた。間葉系幹細胞から心筋細胞へ
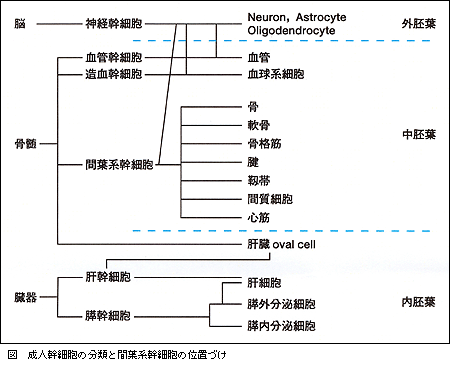
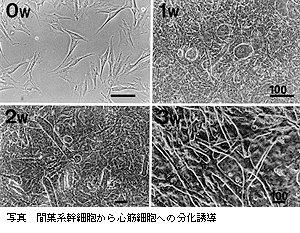
われわれは,骨髄中の間葉系幹細胞と呼ばれる多能性幹細胞が,試験管内で心筋細胞に分化できることをマウスを用いて証明した。骨髄は成体における造血の主たる場所であるが,現在では造血以外の機能も有することが知られている。骨髄中の細胞の99%以上は血球系細胞であるが,1%未満は血球系以外の細胞が存在する。これらの細胞は培養皿に付着する性質を持ち,骨髄間質細胞と呼ばれてきた。骨髄間質細胞は血球系細胞の増殖,分化を促すため,多彩なサイトカインや細胞増殖因子を分泌することが知られている。近年の研究より,この骨髄間質細胞中に多分化能を有する間葉系幹細胞が存在することが報告され,骨,軟骨,脂肪などの細胞に加え,神経細胞や心筋細胞に分化することが明らかとなった。骨髄由来の再生心筋細胞は自律拍動能を持ち,試験管内で毎分120-250回の規則的拍動を行なう。再生心筋細胞の性質を解析すると,胎児期の心室筋細胞の性質を持ち,Na利尿ホルモンであるANPおよびBNPを発現していた。活動電位を記録すると,自律拍動を開始した段階では洞結節様の活動電位が記録されたが,分化が進んだ状態では心室筋様の活動電位を示した。生体内の心筋細胞は交感神経により心肥大が誘発されるとともに心拍数,収縮力,刺激伝導性が増強し,副交感神経によりこれらは抑制される。再生心筋細胞は交感神経α1受容体,β1,β2受容体を発現し,これらの受容体を刺激するとセカンドメッセンジャーの上昇とともに生体心と同様に心肥大・心拍数上昇・心収縮力増強等が観察された。また,副交感神経のM2受容体も発現し,シグナル伝達機能を有していた。
骨髄由来の再生心筋細胞をマウスの成体心に移植した実験では,再生心筋細胞は成体心に生着し,長期間生存することが確認された。さらに,再生心筋細胞は無秩序な方向に配列するのではなく,レシピエント心筋細胞と平行して配列することが認められた。動物実験レベルではこれまで,胎児由来の培養心筋細胞を心筋梗塞症の動物モデルに移植し,梗塞後の心機能の改善に有用であったとの数多くの報告がなされてきたが,ヒトへの応用はドナー細胞の面で現実的なものではなかった。骨髄成体幹細胞を用いた再生心筋の利用はドナー不足,移植拒絶反応,脳死や受精卵使用の倫理的問題などを回避できる利点を有し,再生医療への期待を持たせる画期的な方法である。
今後の課題
今後の課題として,第1に骨髄細胞から多能性幹細胞をいかに効率的に濃縮するか,得られた幹細胞をin vitroでいかに増幅するかという問題があげられる。マウスでは多能性幹細胞をin vitroで継代培養可能であったが,ヒトで可能かどうかは未知の問題である。造血幹細胞の場合は,ヒトではin vitroでの増幅は10倍程度に増幅することが漸くできるようになったのが現状である。間葉系幹細胞で可能かどうか,そのためにはいかなる培養状態が重要かは,今後解決されなければならない問題である。第2に分化誘導法の問題があげられる。われわれが現状で用いているのは分化誘導剤を用いた方法であるが,既知のサイトカイン・細胞増殖因子の組み合わせで心筋への分化誘導が可能かどうかを検討する必要がある。
第3として移植方法の問題があげられる。マウス心臓への移植には注射針を用いて再生心筋を直接移植していたが,ヒトの場合もこの方法でよいのかは改めて検討しなければならない。細胞をシート状にするのか,生体内溶解性高分子スカフォールド上に心筋細胞を載せるのか,血管構築はどうするのかなどを検討する必要がある。これらの技術的に解決しなければならない問題を残しているものの,臨床への応用が見込まれる領域であり,今後の研究の進展が期待される。