新しいリンパ球系NKT細胞
第4番目のリンパ球
| 谷口 克氏インタビュー
千葉大学医学部長,高次機能制御研究センター教授 |
 |
今まで知られていなかったまったく新しいタイプのリンパ球であるNKT細胞。末梢性免疫制御,つまり免疫系統自体の調節を担うこの細胞は,いままでの免疫学における考えを一転させるかのようなトリガーを持つ。
本紙では,その発見者である谷口克氏に,NKT細胞の持つ特性とその発見のプロセスをお話しいただいた。
NKT細胞とは何か
NKT細胞とは,リンパ球系としては新しいリネージ,細胞系列に属する細胞として新しく発見された細胞です。第4のリンパ球ということになります。今まで,リンパ球系列としていわゆるB細胞,T細胞,それからNK細胞の3つが知られていました。B細胞とT細胞が分化して,そのT細胞のリネージの中でさらに2つに分かれます。片方は胸腺にいってT細胞になり,もう一方はNK細胞になるのです。
NK細胞は胸腺外組織で分化し,T細胞やB細胞レセプターのように多様な抗原受容体を発現せず,糖鎖を認識するNK受容体を発現します。T細胞とNK細胞は,まったく独立した細胞系列ですが,同じ前駆細胞(プリカーサ)から分化することが最近明らかになりました。イカロスという転写因子が発見され,その遺伝子を破壊すると,T細胞もB細胞もNK細胞もすべて欠失することから,NK細胞は骨髄系ではなくリンパ球系であることが明確になったのです。
NKT細胞という名前の由来は,今までその発現が相互にexclusiveだと思われていたT細胞抗原受容体と,NK細胞受容体の両方の受容体を発現するという意味で,NKT細胞という名前がつきました。
胸腺形成以前胎生初期に現れるT細胞
NKT細胞が新しい系統といわれる最大の特徴,理由は,通常のリンパ球が発現する以前の胎児組織に出現することです。通常の免疫系の形成は,胸腺ができるのが11日目で,リンパ球の中で最も早いTリンパ球系の出現はそれ以後ということになります。特にαβT細胞が発現するのは,15-17日という胎生後期で,NK細胞やB細胞は生後になって出現します。ですからリンパ球系の生成は,いわゆる生まれる直前から生後にかけて,ということなんですね。 ところがこのNKT細胞は,造血系細胞形成が始まった翌々日あたりから出現します。受精卵の子宮への着床は,マウスでいうと受精後6日目で,その1日-1日半後,いわゆる受精後7-8日ほどで造血系細胞形成が始まるのです。造血系細胞は,yolk sac(卵黄嚢)において骨髄細胞の形成から始まるわけですね。リンパ球も卵黄嚢から派生するという考え方が有力でした。ところがNKT細胞は,大動脈生殖中腎領域という,いわゆる胎児(embryo-body)側から出現することが今回の研究からわかりました。卵黄嚢は,胎児の周りを囲んでいる膜ですが,そこからではなく,胎児側から出現するのです。NKT細胞は他の造血細胞とは違う組織から発生することになります。そういう意味からも,他の細胞から独立した新しい系統であると言っていいかと思います。
たった1つの抗原受容体
NKT細胞が新しい細胞系列であるとする第2の根拠は,NKT細胞の抗原受容体はたった1種類で,NKT細胞だけに発現し,しかもNKT細胞の分化に必須であることが証明されたからです。この受容体はアミノ酸が均一で,本当に1種類しかありません。通常のT細胞抗原受容体は,1015ほどの多様性があるのに,NKT細胞はたった1種類しかないという意味で,この細胞の1つの特徴になっているのです。このNKT細胞抗原受容体は,僕らが1986年に発見して,いちばん最初に報告したVα14という受容体なんですね。免疫制御を専門とする抑制T細胞が選択的に発現しているところから,抑制T細胞の抗原受容体であると当時は考えていました。いずれにせよ,このVα14受容体がNKT細胞だけに発現され,均一で,普通のT細胞には発現しない受容体であることも,この細胞が独立の細胞系列として分類される理由なのです。
このことは次の2つの実験から明らかになりました。1つは,Vα14受容体を強制発現するトランスジェニックマウスを作り,内因性のアルファ鎖遺伝子を欠失させます。こういう状況にすると,アルファ鎖がVα14受容体だけのマウスができます。このマウスを調べると通常のT細胞の分化は完全に抑制され,まったく存在せず,その代わり,NKT細胞だけが発現されます。もう一方は,Vα14受容体をターゲティングによって欠失させたマウスをつくり,NKT細胞だけの消失を確認しました。ですからVα14受容体は,NKT細胞に特徴的で,細胞系列を決定する非常に重要な受容体だということになったのです。
NKT細胞の免疫統御機能
NKT細胞の機能の研究が進み,おもしろいことがわかってきました。最初に発見された機能は,アロ骨髄細胞移植の排除に関係しているものです。このNKT細胞およびNK細胞を除外すると,効率よくアロ骨髄移植が生着することがわかりました。骨髄移植は,遺伝的に適合しない場合,いくらホスト側をX線照射し注射して免疫系を不活化しても,しばらくすると必ず排除されます。骨髄移植を成功させるためには,X線照射だけではだめで,何か処置をしなくてはいけないんですね。これを最初に発見したのは,TakedaとDennertです。その発見は重要だと思います。その後,2番目のNKT細胞の機能を発見したのはNIH(米国立衛生研究所)のPaulらで,NKT細胞が生体の中でIL-4というリンフォカインを作るメジャーな細胞であることを発見したのです。
IL-4自体は免疫グロブリンのクラススイッチファクターで,IgMやIgGを産生するB細胞が,IgEを作る細胞に変換するように仕向けます。これまでの研究ではTh2タイプのヘルパーT細胞がIL-4を分泌するとB細胞に働きかけ,IgEを作るB細胞を増やし,IgE産生が高まりアレルギーを起こすと考えられていました。ですからIL-4というサイトカインは「アレルギーを作るサイトカイン」と言い換えてもいいわけですね。
Th2がアレルギー,つまりIgEを産生させる主役であると思っていたのに,実はそれより1000倍もIL-4を産生する能力を持つ細胞がいたことになり,アレルギー発症に重要な細胞としてNKT細胞が浮かび上がってきたのです。
特に,彼らが主張しているのは,抗原刺激直後に産生されるIL-4サイトカインがアレルギー発症に重要で,それをNKT細胞が作っていることです。したがってこの細胞を除去すると,初期のIL-4産生がほとんどなくなると言っています。実際に僕らのところでNKT細胞を欠失したノットアウトマウスを作り,IL-4産生を見ると,初期のIL-4分泌は起こらなくなることを確認しています。
第3の機能は,われわれ(Miezaらおよび住田ら)が発見したのですが,自己免疫疾患の発症制御にNKT細胞が関係していることです。自己免疫マウスでは,NKT細胞が免疫系から消えてなくなると自己免疫疾患が発病することを見つけたのです。
自己免疫疾患は様々な遺伝子の異常によって起こる多因子疾患で,ほとんどの遺伝子は未だ発見されていません。現在,1つだけ原因遺伝子が判明しているのは,米原・長田グループが発見したFasです。このFasという細胞を殺す自殺遺伝子に異常があると自己免疫疾患が発症することが明らかにされました。そのような原因で自己免疫疾患を発症する自己免疫マウスをlprマウスと呼んでいます。
一方,ニュージーランドブラックマウスとホワイトマウスのF1, BWF1マウスはSLE(全身性エリテマトーデス)様の疾患を起こしますが,原因はわかっていません。Fas遺伝子は正常なので別の遺伝子が関与していることは間違いないのですが。
ところが,SLEや強皮症の患者さん,Fasに異常のあるprマウス,Fasに異常がないBWF1マウスなど全てに共通して言えることは,NKT細胞が免疫系から消えてなくなると自己免疫疾患が発症することです。実験的にも,Vα14受容体を持つNKT細胞を予めなくしておくと,きわめて早い時期から自己免疫疾患が発症することも証明しました。
マウスのVα14受容体とアミノ酸レベルで85%以上の相同性を持つ受容体がヒトにもあります。ヒトの末梢血にCD4, CD8の発現のないダブルネガティブのT細胞がありますが,その細胞のほとんどが,均一なVα24JαQ受容体を発現しているのです。
健康人は均一なVα24JαQ受容体を持つNKT細胞がドミナントになっています。しかし,自己免疫疾患のSLEあるいは強皮症の患者さんは,このVα24T細胞がないのです。これはマウスとヒトで共通にみられる現象で,NKT細胞は自己免疫疾患の病態をコントロールする中心的な細胞であると思われる理由なのですね。
免疫系をコントロールする
NKT細胞は免疫系をコントロールしている細胞であることがわかってきました。では,それが免疫系をどのようにコントロールしているかが最大のポイントになります。しかし,その問題については,in vitro での実験しかなされていないのです。 これまで知られているT細胞によるサイトカイン統御は,ヘルパーT細胞Th1とTh2による統御です。Th1はγ-IFNとIL-2を,Th2はIL-4, IL-10などを産生します。ところが,このNKT細胞はIL-4のほか,γ-IFNも産生します。いわゆるTh1とTh2タイプのサイトカインの両方を産生することになるのです。さらに,Vα14T細胞受容体を刺激するとIL-4が産生され,NK細胞受容体を刺激するとγ-IFNが産生されることを千葉大の荒瀬尚君が見つけています。NKT細胞は相手によって産生するサイトカインが異なり,免疫反応の様式がまったく違ったものになります。そのほかにNKT細胞はFasリガンドを発現していますから,Fas受容体を介する細胞障害活性も示します。さらにパーフォリンも産生し,NK細胞のような活性も出します。
免疫統御において,たった1個の武器を使うのではなく,相手を見ていろいろ武器を変えてしまう,知能的な動きをするのです。いわゆるTh1,Th2バランスをコントロールすることで免疫制御する方法と,Fas受容体を介する細胞障害を起こす方法,それから,パーフォリン依存性の細胞障害を起こす方法,この3つの武器を使い分けています。しかし,これらはin vitro で確かめられたもので,in vivo でどのような病態のときにどういう使い分けをしているかについては,まだわからないのです。
さきほどVα14受容体トランスジェニックマウスの話をしましたが,教室ではNKT細胞マウスと呼んでいます。このマウスではT細胞の分化はブロックされ,コンベンショナルなT細胞は分化されず,全部NKT細胞になり,この細胞の機能を調べるにはNKT細胞マウスが最も適しています。何しろNKT細胞しかないマウスですから。このマウスを用いてNKT細胞のin vivo機能が明らかになるでしょう。
NKT細胞発見のプロセス
私は基本的に,免疫系にはプラスの反応とマイナスの反応が必ずあると考えています。というのも,すべての現象にはプラスとマイナスがあるからです。だから,「スイッチオン」するものがあれば,「スイッチオフ」するものがある。システムがきちんとシステムとして成り立つためには収斂・統御・統制する力が必要です。いかに制御するかによって,そのシステムとしての特徴も決まるわけです。免疫系のように,ものすごく多様で,1015の役者が揃っている場合には,やはり「制御するメカニズム」がいちばん重要なのですね。あんなにみごとに調和が保たれているのに,役者がたくさんいて,1つの演劇のプロローグからエピローグまで,統一のとれたストーリーを作り出すためには,統制が行なわれない限り不可能です。僕は昔から,そういう意味で免疫制御のことを研究しているのです。
NKT細胞のいちばん特徴的な受容体Vα14の発見は,私が多田富雄先生(現東京理科大生命科学研)と一緒に研究していたころ,抑制T細胞ハイブリドーマを数多く作成し,その受容体遺伝子を調べていたところに端を発します。別々に作成した13株のハイブリドーマをすべて調べたら,そのうち12株が同じVα14受容体遺伝子を使っていたんです。ハイブリドーマはモデルですから,アーチファクトかもしれないと考えられたのです。ハイブリドーマで見つけた均一なVα14受容体が本当に生体に存在し,意味があるかどうかを逆に検証することによって見つけていきました。 ですから,免疫制御のメカニズムを知るためにあきらめずにいたことが,こういうおもしろい細胞の発見につながったのではないでしょうかね。要するに,免疫制御にはいろいろな制御の仕方があり,Fas,パーフォリンなどの細胞傷害機構で標的を殺すことで制御する場合もあり,TGF β(transforming growth factor)や,あるいは石坂公成先生がやっておられるような抗原特異GIF(glycosylation inhibitory factor)のような抑制サイトカインが作用する場合もある。ですから,この細胞に名前をあげるとすれば,「免疫統御細胞」というのがよいと思います。この細胞は免疫系を統御することが専門ですから,この細胞の司る免疫統御システムは,感染防御系に対比するものとしての存在を証明したことにもなると思うのです。
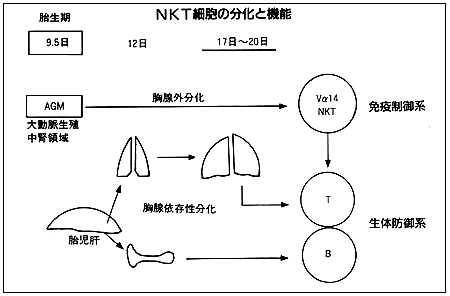
免疫系を制御する専門家
NKT細胞は,他のリンパ球とはまったく別の経路で分化します。すなわち,NKT細胞の分化に胸腺は必要ないのです。NKT細胞はリンパ球上の自己成分を抗原として認識し,免疫反応を制御しているのです。自己を見ているということは,胸腺で分化するシステムだと,特別なメカニズムがないかぎり,胸腺の中で殺されてしまうわけでしょう。したがって,「胸腺外分化」のプロセスを通るのは,免疫統御系の必然的な分化のシステムだと思います。NKT細胞の機能に関して,私は2つのドグマを考えています。1つは,この細胞は造血系を標的にしていますが,「胎生の非常に初期,つまり免疫系の存在しないうちは造血系をシェイプアップするために大きな役割を担っているのではないか」ということです。Vα14受容体遺伝子ノックアウトマウスを調べて,造血系に変化が起こるかどうかで見極められると思います。
2番目の可能性は,「NKT細胞を中心とする免疫制御系が免疫系のプロトタイプではないか」ということです。その理由は,(1)NKT細胞分化に胸腺を必要とせず,しかも胸腺形成前の胎生初期から出現すること,(2)受容体はただ1種類で,それは「自己」を認識し,相互作用を行なうものであること,などです。
生体にはもともと,NKT細胞しか存在しなかったが,ウイルスやバクテリアのような外来異物に対処するために,リンパ球のレパートリーと数を急激に増やす必要に迫られて胸腺を作り,胸腺依存性の免疫系を作っていったと考えられるからです。
NKT細胞が認識する抗原はCD1非MHC分子
最近,Bendlacらが,「NKT細胞の認識するMHC分子はCD1だ」と明らかにしました。これが本当にCD1かどうかということは,これから検証されなければいけないのですが,このMHC分子は非常にmonomorphicで,マウスには1種類しかなく,すべて共通です。それからヒトのCD1はA,B,C,Dタイプと4つあるのですが,マウスのCD1に相当するのはCD1Dで,これもヒトすべてに共通です。先ほど,どんなHLAのタイプの人でも,invariantなVα24JαQ受容体は持っているとい言いましたが,マウスでもすべての亜種がVα14受容体を高頻度に持っています。それはmonomorphicなMHCが抗原を提示して,それを認識しているから当然のことと言えます。まだ先の話ですが,均一なVα14受容体のみを発現するNKT細胞を標的にした自己免疫疾患の治療の可能性が考えられます。NKT細胞の選択的減少が自己免疫発症の原因とも考えられますから,Vα14受容体のリガンドを同定すれば,NKT細胞を活性化したり,前駆細胞から成熟型への分化を促したりして自己免疫疾患の治療法の開発にもなると思われます。ですから,Vα14受容体のリガンドを発見すれば非常にいい薬になります。しかもみんなに共通で,誰にでも使えますから。
造血系を標的とした統御
次の最大の研究のターゲットは,in vivo でNKT細胞がどういう武器を使って,どのような統御をしているか,免疫系においてどのような役割を担っているかということです。これまで胸腺依存性の免疫系だけで物事を考えようとしていたけれど,もっと発生学的に古い,別の系統がいて,そちらのほうがプロトタイプかもしれないとすれば,免疫そのものの概念が変わりますね。免疫系の本来的な意味は,造血系全般のコントロールだったかもしれない。自分の造血系を作るとき,造血系から異常細胞を取り除き,シェイプアップするための役目だったかもしれないのです。NKT細胞の発見は1987年で,僕らが均一なVα14受容体を見つけた翌年に,NIHのFoulkesらが,胸腺中に変な細胞がいると発表しました。Tリンパ球なのにNKマーカーを持つ変わり種ということで,ある人はそれに注目したけれど,あまりにもminor population(胸腺中に0.4%)なためよくわからず,ほとんどそのままになっていたんですね。
ところが,Vα14はNKT細胞の唯一のマーカーで,それを指標に調べてみると,肝臓や骨髄だと50%のT細胞が,脾臓ではT細胞の5%を占める大集団であることがわかりました。肝臓や骨髄の造血にかかわる臓器に,必ず大量に存在するのです。このことから,NKT細胞の機能的役割が造血系を標的にした統御であることは十分納得できることです。
NKT細胞研究に寄与した技術
この研究において最も有効だった技法は2つあり,RNaseプロテクション法とPCR法です。RNaseプロテクションアッセイを用いて,NKT細胞がin vivo に大量に存在し,機能することを見つけたのは,当時大学院生だった古関明彦君です。RNaseプロテクション法は,多くの物の中から特定のmRNA量を定量するのに優れた方法です。この技術がなかったら,Vα14受容体が生体内で意味のあるものか否かわからなかったでしょう。それからPCR法ですね。特にPCR法は1コピーの特定の遺伝子を目に見えるくらい大量に増やすことが可能な技術です。目に見えないマイナーな生理活性物質が大きな機能である免疫系では,この技法はことさら有効でした。また,NKT細胞の発生するきわめて早い時期(胎生9.5日)を同定できたのも,このPCR法のおかげです。
NKT細胞にだけ発現されるVα14受容体は,1986年にT細胞ハイブリドーマから単離されたことは最初にお話しました。そのとき,13株のうち12株のハイブリドーマ細胞がこのVα14受容体を発現していたために,免疫制御系に特有の受容体だと思っていました。これが生理的に意味のあるものか否かを知る唯一の方法がRNaseプロテクション法だったのですね。
普通は,T細胞受容体アルファ鎖のレパートリーは108くらいですから,ある特定の受容体の頻度は108分の1になり,RNaseプロテクテション法では検出できません。しかし,もし数%存在するのならばバンドとして目に見えるはずだと考えたのです。
ですから,この予想が当たっているとすれば,in vivo に絶対にバンドとして見えるはずだからとやってみたら,本当にバンドが出たのです。あれはもう感激だった。粘り勝ちというところですかね。新しい発見や,研究なんてこんなものかもしれません。


