異分野融合の先に広がるがんDDS研究の展望(松村保広,西川元也,西山伸宏,我妻利紀)
対談・座談会
2019.01.07
【座談会】
異分野融合の先に広がる
| |
 | |
|
異分野連携を重視する考えは,今や学術界では常識となっている。DDS研究はその常識に先駆け,1980年代から,広範な学問領域にわたり分野の壁を取り払った議論を続けてきた。学際的な知見をもとにしたがんDDS治療薬開発に向け,各分野の研究者はどのような将来を見据えているのか。医学,薬学,工学,企業の研究者の4氏による座談会では,分野の枠組みを超えた「擦り合わせ」が生み出す新たな治療薬開発の展望が語られた。
松村 がん薬物療法は着実に進歩を続けています。その進歩は,がんの病態の解明と新規薬物の発見だけでなく,疾患部位だけに薬物を送達するDDS研究の発展に支えられてきました。がん組織にIgGが集積しやすいとの病態生理学的特徴をEPR(Enhanced Permeability and Retention)効果1)として私が報告したのは1986年のことです。以来,DDS研究はEPR効果を理論的支柱に,多分野の研究者を巻き込みながら急激な発展を遂げています。
「疾患部位に薬を届ける」を共通の目標に
松村 議論に先立ち,DDS研究を始めたきっかけと現在の専門をご紹介いただきます。私は熊本大医学部を卒業後,後に世界初の高分子抗がん薬となるスマンクス/リピオドール動注療法の研究が縁で,前田浩先生(当時・熊本大大学院)に師事しました。おかげでEPR効果発見の論文を世に出すことができました。現在まで高分子を用いたがんDDS研究を続けています。
西川 私のDDSとの出会いは薬学生時代でした。日本DDS学会初代理事長の故・瀨﨑仁先生(当時・京大)の研究室に所属したのがきっかけです。これまで一貫して,生物薬剤学,薬物動態学に立脚した疾患治療システム開発に取り組んでいます。生理活性タンパク質や抗原ペプチド,核酸などの高分子の体内動態をいかに制御するかを考えてきました。
現在の研究テーマは核酸のデリバリーです。DNAナノテクノロジー(図1)と,細胞が産生する小胞であるエクソソームを用いたDDSを探究しています。生体とマテリアルの特徴を踏まえた体内動態制御をめざしています。
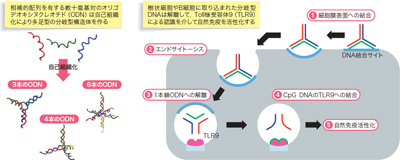 |
| 図1 DNAナノ構造体の研究(クリックで拡大) |
| 核酸医薬が効果を発揮するには細胞内に取り込まれる必要がある。核酸は相補的な配列の工夫によって天然には存在しない分岐型構造を取ることもできる2)。分岐型構造の核酸は免疫細胞に取り込まれやすい特徴を持ち,メチル化されていないシトシンとグアニンが連結した配列(CpGモチーフ)を含む場合には免疫応答を亢進する。 |
西山 工学系出身である私も恩師の指導を受けて今があります。大学院ではナノキャリア研究の第一人者である,片岡一則先生(川崎市産学振興財団ナノ医療イノベーションセンター)の研究室に入りました。その後,ポリマー薬剤研究のパイオニア,Jindřich Henry Kopecček先生(米ユタ大)にも教えを受けています。これまで高分子ミセルを中心に,抗がん薬,核酸医薬,タンパク質等のデリバリーを研究してきました。
2013年に東工大に移ってからは,既存の素材を使うだけでなく,新材料の創出にも力を入れています。がん治療薬に加えて,診断薬も研究対象です。
我妻 私は薬学生時代に,故・橋本嘉幸先生(当時・東北大)の研究室で,がん治療,特にがん免疫療法に関連した研究に携わりました。1991年に製薬企業に入社後,抗HIV薬や抗がん薬,ゲノム創薬の研究などに従事しました。2000年頃からは抗体医薬の研究基盤作りと開発パイプライン拡充を進めています。
最近は次世代抗体医薬,特にADC(Antibody-Drug Conjugate;抗体薬物複合体)の自社技術開発に力を入れてきました。ADCは抗体医薬の発展系であるとともに,抗体を使って抗がん薬を標的がん細胞に選択的に送り込むDDSの一つです。
松村 それぞれバックグラウンドは異なるものの,疾患部位にだけ薬物を届けるシステム作りをめざしている点は共通ですね。
分野を超えて同じ志を持つ者が連携し,新しい技術を生み出してきたのはDDS研究の特徴です。かつて,片岡先生と医学・工学の共同研究を始めたときのことをよく覚えています。きっかけは,とある工学系研究会で,片岡先生がEPR効果に言及したのを私がたまたま聴講したことでした。DDS研究の異分野連携・異分野融合は政策によるトップダウン型ではなく,一人ひとりの研究者が築いてきたボトムアップ型の文化なのです。
がん治療薬開発に,DDS研究が欠かせない時代を迎えています。がん薬物療法の大きな流れとともに振り返ってみましょう。
体内動態を精密に制御できる基盤技術として注目されるDDS
松村 がん薬物療法が始まって以来開発されてきた低分子の化学療法薬は,治療域が狭く,骨髄抑制など生命にかかわる副作用が出やすい欠点が治療上の制約になっています。がん細胞だけでなく正常細胞も攻撃してしまうからです。
その後,がん細胞のみを攻撃する発想から分子標的薬や抗体医薬が登場しました。中でも抗体医薬の開発が進み,国内外で製品別売上高の上位を占めるようになっています。抗体医薬の隆盛を,企業の立場からどう見ますか。
我妻 効果・副作用の両面で優れていることが普及の理由でしょう。正常細胞では発現せず,がん細胞だけで活発に働く分子機構の制御を狙った薬です。適切な患者さんに投与すれば,効き目は非常に良く,副作用は従来の薬よりも少ないです。
製薬企業の視点からは,分子群の枠組みに縛られない新たな創薬アプローチでもありました。従来は低分子医薬品が創薬の中心で,標的にできる分子群は受容体や酵素などに限られていました。複数の企業が同じ分子群を標的に薬を開発して競合することも多く,独自性の高い医薬品創出という観点から抗体医薬が注目されたのでしょう。
松村 高い標的選択性を持つ高分子として,抗体の有用性は以前から認識されていたとも思います。製薬企業にとっては,抗体を作る抗体工学領域の進歩も大きかったのではありませんか。
我妻 その通りです。ヒト体内での免疫原性によって排除されてしまう問題や,均質な工業製品として製造する難しさがあり,医薬品としての開発は長らく停滞していました。1990年代の抗体工学の技術革新により,免疫原性の低い抗体を精密に設計し,均質に大量生産できるようになりました。この革新により,抗体医薬が続々と上市される時代が来たと考えています。
松村 こういった背景で広まってきた画期的な抗体医薬も,がん治療の分野ではいくつかの限界が明らかになってきました。
我妻 がんは遺伝子変異を繰り返しながら増殖し,性質の異なる細胞が集まっていると考えられています。そのため,特定の標的分子の識別に頼る戦略では,その標的分子が変異したがん細胞は攻撃から逃れて生き残ります。結果として薬に耐性を持つがんとなって再発してしまうのです。がん細胞に対抗するには,「heterogeneity(不均質)の壁」があるのです。
西山 非常に大きな課題です。一時は劇的に効いても,再発により数か月しか延命できないことも多く,がんの根本治療には至りません。
西川 そこで,新たなアプローチで体内動態を制御するDDSが注目されてきたのでしょうね。
我妻 実臨床でDDSの有用性を裏付ける報告も出てきて,DDS製剤への見方は以前にも増して前向きになってきたのではないでしょうか。例えば,当社が開発中のADCは,日米の規制当局から優先的な審査を受けています。
松村 いうなれば,DDS研究がもたらす,がん治療の革新へ期待が高まってきたということです。西川先生,新領域と見込まれる核酸医薬では,DDSはどのような位置付けですか。
西川 核酸医薬開発でもDDSの注目度はかなり高いです。2018年8月に,米FDAと欧州EMAは,hATTRアミロイドーシスの治療薬patisiran(Alnylam Pharmaceuticals社)を承認しました。世界で初めてRNA干渉(RNAi)を利用した本剤は,脂質ナノ粒子が核酸を内包する構造です。核酸医薬で初のDDS製剤という点も特筆に値します。
松村 Patisiranは遺伝子疾患への核酸医薬で,日本でも近く承認されそうです。
西山 核酸医薬は夢のある分野と私も感じています。標的細胞の中まで届ける技術の開発が鍵なので,DDSが特に重要と分析しています。
西川 全く同感です。従来,開発の壁といえば,核酸医薬の生体内安定性の確保でした。近年,核酸修飾技術の進展で解決に向かい,脊髄性筋萎縮症に使われる髄腔内注射薬ヌシネルセンなど,少数ながら臨床応用されています。
負電荷の高分子である核酸は元来,生体膜をほとんど透過しません。標的細胞の中まで核酸医薬を運ぶDDSこそ,現在の最大の課題です。2018年10月時点で,がんに適応を持つ核酸医薬はありません。しかし海外では臨床試験が始まっているので,いずれはがんを治療する核酸医薬も出てくると思います。
西山 これまで,薬物送達を扱うDDS研究を製剤領域と見なして,新薬開発と切り離して考える場合が多かったのではないでしょうか。しかし,核酸医薬など精密な体内動態制御が求められる薬の開発が進む今,高機能なDDSは新薬の設計段階から欠かせません。いわば,DDSは医薬品開発の基盤となる技術なのです。
松村 抗体医薬が短期間で一般化したように,DDS研究はがん治療を一新する可能性を秘めています。次々と考案される治療法の実用化を,DDS研究が推進する原動力となるのは間違いありません。
薬を運ぶ「入れ物」から,診断機能を併せ持つ「ナノマシン」へ
松村 現在の研究を交えながら,DDS研究ががん治療にどのような革新をもたらすかをお話しください。西山先生の研究は実用化に近いと聞いています。
西山 はい。シスプラチン内包ミセル製剤NC-6004(関連記事・表)など,2つのミセル型DDS製剤でPhase III試験を進めています。ミセルは材料によって性質を変えることができます。単なる“薬の入れ物”ではなく,例えば外殻には,生体から異物と認識されにくい材料を用いる工夫をしています(図2)。
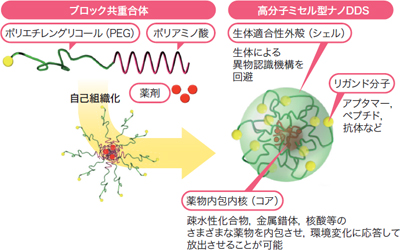 |
| 図2 ミセル型DDS製剤(クリックで拡大) |
| 開発中のミセル型DDS製剤の仕組み。ミセルは,両端で性質の異なる分子が自己組織化により集積したもの。血中滞留性を高めるため,外殻(シェル)は生体に異物と認識されない工夫がなされている。薬物は内核(コア)に分子間相互作用によって保持される。 |
西川 どのようにがん組織へ集積し,内包した薬物が放出されるのですか。
西山 腫瘍への集積はEPR効果によります。直径20 nm程度と,腫瘍内分布に適した大きさに調整しています。腫瘍への集積後,ミセルがゆっくりと崩壊し,薬物が放出されます。
松村 ミセルを利用した初のがんDDS治療薬として,臨床試験の行方が気になります。
同じくナノ粒子であるリポソームでは,すでに多くの医薬品が開発されています。リポソーム型DDS製剤の特徴は,生体内での高い安定性です。腫瘍集積性と血中滞留性を両立できるのは魅力的です。2017年にFDAが承認したダウノルビシン・シタラビン内包リポソーム製剤(CPX-351,関連記事・表)では,薬物をリポソームに入れた群で有意な治療効果の改善が見られました。この成果は血中滞留性の向上が大きく寄与したのではないかと考えています。
西山 試験結果は興味深かったです。既存の医薬品をDDS製剤化しただけの違いで,効果が高まったからです。
松村 リポソームと同じ脂質二重膜の粒子体,エクソソームについてはいかがでしょう。
西川 エクソソームは細胞間情報伝達に機能すると見いだされて以来,運搬体として活用が模索され始めました。現状は体内動態がわかりつつある段階で,実用化はまだ先です。いずれはエクソソームを利用した医薬品も登場するかもしれません。
我妻 企業もナノ粒子の研究に着目しています。治療にとどまらず,診断のDDS研究も進んでいるようですね。
西山 はい。ナノ粒子で治療薬をデリバリーするDDSだけでなく,より高度な診断機能も併せ持つ「ナノマシン」への進化をめざしています。
有望な用途は造影剤です。ナノ粒子の腫瘍への集積性を利用するだけではありません。研究中のDDS製剤は,がん組織のpHが正常組織より低いことに着目し,低pH環境下でマンガン造影剤を放出する機能を備えています。これまで普及型の低価格MRIでは検知が難しかった1.5 mm程度の微小がんを,高感度に検出できる可能性があります(図3)。
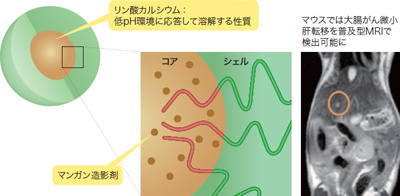 |
| 図3 従来型ナノ粒子の機能を強化した「ナノマシン」造影剤(クリックで拡大) |
| マンガン造影剤を搭載したナノマシン。血中(pH 7.4)とがん組織(pH 6.5~6.7)の違いに着目し,疾患部位のみで造影剤を放出する。マウスへの投与では,これまで難しかった1.5 mm程度の微小がんを,広く普及している安価な1テスラMRIで検出できたという。 |
診断だけでなく,DDS製剤投与前にナノマシン造影剤を用いれば,患者ごとにナノ粒子DDS製剤の集積性を予測できます。効果の見込める患者を事前に見極める,高度に個別化されたプレシジョン・メディシン(精密医療)のコンパニオン診断薬となる可能性を秘めています。
西川 治療薬の運搬に着目してきたDDS研究の枠組みを広げる発想は魅力的です。薬物のデリバリーだけでなく,診断の精度を高め,治療効果を感知する総合的な治療システムとして,DDSの進歩に期待しています。
「擦り合わせ」の力で新時代を迎える抗体医薬
松村 続いて,抗体を使った新たなDDSについて話したいと思います。中和抗体として用いるだけではない,抗体医薬の可能性についてお話しいただけますか。
我妻 がん細胞に特有の分子に対する抗体の特異性だけに頼る戦略に,限界があるのは先ほど議論した通りです。そこで,抗体を直接的に薬として使うのではなく,低分子の抗がん薬をがん細胞まで届ける「運搬役」として用いるADCが合理的なアプローチとして注目されるようになりました(図4)。当社では1999年頃から新技術を搭載したADCの研究開発を行ってきました(図5)。
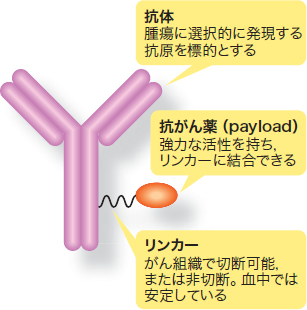 |
| 図4 ADC(抗体薬物複合体)の構造 |
| 選択的かつ効果的にがん細胞を攻撃することで,既存の化学療法薬と比較して効果が強力かつ,広い治療域が期待される。 |
 |
| 図5 バイオ医薬品新薬研究の展開(クリックで拡大) |
| 1990年代から盛んに開発されてきた抗体医薬は次のステージへ向かっている。抗体そのものを薬として使うだけでなく,抗体工学技術を生かした創薬をめざしている。 |
松村 ADCの開発が近年,かなり活発になった理由は何ですか。
我妻 抗体の作製,搭載する低分子抗がん薬(payload)の選定,抗体とpayloadをつなぐリンカー技術,それぞれの技術革新です。ADCは世界ではすでに数品目が承認されました。
しかし,まだ改良の余地はあります。ADCはグローバルの中で,日本のものづくりの強みを生かせる分野だと思います。複合的な技術の擦り合わせによる技術革新は日本が得意な分野です。精密な技術の最適化と擦り合わせは簡単ではありませんが,多くの専門家が膝を突き合わせ,根気強くtry and errorを繰り返すことで,良いものづくりができるでしょう。
当社では,膨大な試行錯誤の結果を踏まえ,細胞膜透過性の高いpayloadを採用しました。細胞膜を透過しやすい抗がん薬を搭載すれば,標的分子を発現していないがん細胞も攻撃できるのです。従来の抗体医薬の枠を超えた,画期的な仕組みです(図6)。
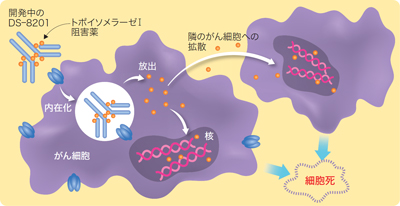 |
| 図6 バイスタンダー効果(クリックで拡大) |
| がん細胞内で遊離した抗がん薬が細胞膜を透過し,周囲のがん細胞にも作用する効果。これにより,抗原が発現していないがん細胞も攻撃することができる。 |
西山 バイスタンダー効果と呼ばれるものですね。確かに,これなら従来の抗体医薬が課題とするheterogeneityの壁を克服できるかもしれません。
我妻 化学療法薬は細胞毒性が高く,がん細胞の破壊に効果的です。抗体を運搬役とすることで化学療法薬を局所に集積させるADCは,がん治療の新しい地平を開くのではないでしょうか。
松村 細胞内に取り込まれるのではなく,がん細胞近傍に存在する間質に特異的な抗体で抗がん薬を運び,細胞外で抗がん薬をリリースするがん間質ターゲティング(Cancer Stromal Targeting;CAST)療法も,同様に抗体を用いた新たな戦略です(図3参照)。標的は遺伝的に保存性が高い不溶性フィブリンです。不溶性フィブリン表面でのみ活性化されるプラスミンで切断される特徴を持つリンカーが鍵で,この部分は有機化学が専門の眞鍋史乃先生(理研)に作製していただきました。膵がんなど,間質が豊富で高分子ががん細胞まで到達しにくいがんへの対抗手段として期待しています。
西川 がん組織まで選択的に到達するのが高分子の強みで,高分子では難しいがん組織内での拡散性が低分子の強みですね。それぞれ単独では難しい体内動態の制御を,高分子と低分子の組み合わせによって実現する点はナノ粒子もADCも共通しています。
松村 思いがけない組み合わせとして,放射線免疫療法の研究も始まりました。抗体にα線放出物質を付けるものです。新元素ニホニウムを発見した理研の研究グループの一人,羽場宏光先生と現在,共同研究を進めています(関連記事)。
α線は強力な放射線であるものの,飛距離が短く,これまでがん放射線療法の主力ではありませんでした。しかし,がん局所に運ぶDDSと融合すれば,全く新しい放射線療法が誕生します。DDS研究の異分野融合は,医学,薬学,工学などにとどまらず,核物理学といった新たな分野にまで及んでいます。DDS研究によって,がん治療法開発の夢はますます広がります。
臨床応用を踏まえた課題を探る
松村 しかしながら,実用化までには課題もあります。DDS製剤の開発を成功させ,臨床に届ける上で,課題は何でしょうか。
西川 遺伝子の発現制御を主目的に開発されている核酸医薬は,細胞内まで薬を届けるシステムの構築が研究途上です。
我妻 核酸医薬はがん領域に限って言えば,実用化に時間がかかると見ています。遺伝子発現の不足による遺伝性疾患では,一部の細胞に核酸医薬が届き,機能を回復できれば病態の改善が見込めます。しかし,がんでは全てのがん細胞に核酸医薬を届け,がん細胞を破壊するアプローチが必要ですよね。
西川 おっしゃる通りです。効果をin vitroで確認できても,in vivo,ましてや臨床応用化の壁が厚い理由は薬物送達の効率性が課題だからです。
一方で,ヒトの樹状細胞やB細胞に発現する受容体を介して自然免疫を高める免疫アジュバントの特徴を持つ核酸もあります。がん細胞に届けるだけでなく,免疫細胞へのデリバリーなどにも核酸医薬は応用の可能性があります。そこで,ナノ粒子に核酸医薬を搭載する方法だけでなく,免疫細胞に取り込まれやすいDNAナノ構造体の研究を進めています。
ただ,核酸を認識する受容体はヒトとマウスで種差があり,マウスでの評価をヒトに外挿できるかどうかの検証が必要です。
松村 実験動物とヒトの種差は,ヒトでの実用化を前提にした研究を進める上で大きな課題ですね。組織の性質も異なるところが多いです。
西山 そうですね。腫瘍モデルマウスには高分子の浸透を妨げる間質がほとんどないのに対し,ヒトのがんの多くには間質が存在します。高分子の動態の違いには悩まされています。
松村 よりヒトに近いモデルの開発の他,種差の少ないターゲットを探索する戦略もあるでしょう。DDS製剤は,腫瘍への集積と薬物の放出という2段階の最適化が必要です。いずれも,ヒト組織に最適化した開発が肝要です。
西山 理想的には,DDS製剤にイメージング機能を搭載し,ヒト体内でどのように集積するか明らかにできれば,治療効果の確実性は高まるでしょう。例えば,ホウ素を用いた中性子捕捉療法では事前にPETを使って腫瘍へのホウ素の集積度を確認し,患者を選別して治療しています。研究・治療の双方の見地から,効果予測を可視化する機能を持つDDS開発が必要です。
我妻 どんな患者さん,どんながん種で治療効果が出やすいかを知ることは医薬品を作る上でも基本です。臨床試験に参画いただく患者さんを決める,開発戦略の基盤にもなります。
西山 さらには,ポリエチレングリコール(PEG)などの既存の素材を組み合わせるだけでなく,より高機能化した新規材料の開発も重要でしょう。PEGを用いた既存のナノ粒子は生体の異物認識機構を回避するpassive targetingの手法が軸ですが,現在,がん細胞への選択性を持たせたactive targetingの戦略も考えています。
例えば,正常細胞とがん細胞に発現するグルタミントランスポーターの密度の違いに着目しています。グルタミントランスポーターに親和性の高い高分子材料をPEGの代わりに用いることで,シンプルかつ高機能なDDS製剤開発をめざしています。
松村 実用化の観点からは,一定の品質の製品が大量に作れるかという製造の視点も重要です。DDS研究の最終的な出口は臨床応用です。社会に薬を届ける企業の役割も欠かせません。
我妻 抗体医薬は製造プロセスが確立し,市場が受け入れ可能な価格で製品化できたのが普及した理由の一つです。大学の研究者が行う研究は挑戦的なものが多いです。企業の立場からは,大学の研究者の発見を社会に還元する突破口を開く,製造法の研究も不可欠と感じます。
西山 DDS研究の真の価値は論文を書くことにとどまらず,実用化して患者に届けること。実用化にはヒトでの有用性を確認するだけでなく,質・量を規格化し,製造基準を満たし,コストを許容範囲に抑えなければなりません。高機能でも複雑な仕組みでは実用化は困難です。優れた機能をシンプルな構造に凝縮する研究にこそ,真の価値があると言えます。
多領域の知見を結集し,新しい治療を開く
松村 今後,DDS製剤はがん治療の切り札の一つになるでしょう。DDS研究者として,がん治療を変える夢を語っていただきたいと思います。
我妻 がん治療薬の到達点は一時的な延命ではなく,健康な社会生活を送れる状況を長期に提供することです。これを何としても,実現したい。
西山 同感です。がんを根本的に治すには,ピンポイントに薬物を運ぶ発想が,やはり必要です。新しい薬をゼロから創るだけでなく,がんに治療効果を持ちながらも全身の副作用で実用化できなかった薬物にとって,DDSは福音となる可能性を持っています。疾患部位にだけ薬物が届けられれば,副作用の発現を抑えられるからです。
西川 また,体内の薬物動態を制御し,「必要なときに,必要な場所に,必要な量の薬物を届ける」というDDS研究の原点に立ち返れば,患者の治療にかかる時間的・費用的負担を減らす改良もできるのではないでしょうか。
松村 がん治療の進歩で長期生存する患者が増えた今,治療の改良にも社会的なインパクトがありますね。治療の場を入院から外来へ移し,さらに受診回数を減らすなどの工夫は必要です。DDS研究の進歩は,がん治療の成績向上にも,生活とがん治療の両立にもつながります。そんな未来を,DDS研究はもたらしてくれるのではないでしょうか。
私が感じるのは,DDS製剤と既存の治療法の組み合わせが持つ可能性です。研究者は自分の研究領域に凝り固まって結果を出そうとしがちです。しかし,DDS製剤と既存の治療法の組み合わせが良い成果を出したとの報告は相次いでいます。
西山 高分子ミセル型DDS製剤と免疫チェックポイント阻害薬の併用など,学際的な研究も進展しつつあります。分野横断的な技術の融合で,がん治療に革命的なイノベーションが実現できるのではないかと思います。連携の可能性は無限です。常にアンテナを張っています。
我妻 DDSは産学の研究者の努力で進化を続けてきました。今後,DDS研究では産学連携の重要性がさらに高まるでしょう。企業とアカデミアで立場は違いますが,患者さんに素晴らしい医療を届けたいとの思いは共通です。イノベーション創出国として日本がさらに発展するためにも,これまで以上の密な連携が大事だと考えています。
西川 研究では,核酸はDDSで運ばれる側だけでなく,DDSの素材としても使えることがわかってきました。これまでにないDDS技術開発に向け,アイデアを一つひとつ積み上げていき,患者さんに良い医薬品を届けたいと思います。
西山 疾患部位だけに作用する医薬品の追求は将来にわたって続くでしょう。DDS製剤を一つでも多く世の中に送り出し,いち早く普及に努めるとともに,世の中にまだないDDS技術を開発する長期的視座に立って研究に邁進します。
松村 本日はそれぞれの立場から,DDS研究の連携・融合を語り合いました。ナノスケールの研究領域であるDDSに,研究者・医療者・患者の大きな夢が詰まっています。DDS研究が開く,がん治療の未来は明るいものとなるでしょう。皆さま,本日はありがとうございました。
(了)
参考文献
1)Cancer Res. 1986[PMID:2946403]
2)Adv Drug Deliv Rev. 2010[PMID:20230867]
 まつむら・やすひろ氏
まつむら・やすひろ氏
1981年熊本大医学部卒。同年より同大病院第一外科。88年同大大学院博士課程修了,博士(医学)。89年米マウントサイナイ医科大腫瘍内科,90年英オックスフォード大ナフィールド病理ポストドクトラルフェローなどを経て,94年国立がんセンター(当時)中央病院。2002年より現職。ADC新規開発をめざす株式会社凜研究所研究担当取締役を併任。1986年にEPR効果を発表し,同論文が2016年,トムソン・ロイター引用栄誉賞を受賞(18年8月時点で被引用回数5500回以上)。18年から日本DDS学会理事長を務める。
 にしかわ・まきや氏
にしかわ・まきや氏
1990年京大薬学部卒。95年同大大学院薬学研究科博士後期課程単位取得退学。96年博士(薬学)。同年より同大薬学部助手。99年米ピッツバーグ大博士研究員。2002年京大大学院薬学研究科病態情報薬学分野准教授。17年より現職。生物薬剤学・薬物動態学を基盤に,生理活性タンパク質や抗原ペプチド,核酸など医薬品への応用が期待される高分子化合物のターゲティングシステムの開発に取り組んでいる。
 にしやま・のぶひろ氏
にしやま・のぶひろ氏
1996年東京理科大基礎工学部卒。2001年東大大学院工学系研究科材料学専攻博士課程修了,博士(工学)。同年,米ユタ大薬学部博士研究員。03年東大病院ティッシュ・エンジニアリング部助手。同大大学院医学系研究科疾患生命工学センター助手,講師,准教授を経て,13年より現職。東京理科大,東大大学院ではナノキャリア研究の第一人者である片岡一則氏のもとで研究経験を積んだ。臨床試験中のシーズを複数開発した実績を持つ。
 あがつま・としのり氏
あがつま・としのり氏
1989年東北大薬学部卒。91年に三共株式会社(当時)に入社し,同社バイオサイエンス研究所に配属。94年英MRC collaborative centreにて抗HIV薬の研究に従事。東大医科研を経て第一三共株式会社創薬基盤研究所,抗体医薬研究所等に勤務。2013年にバイオ創薬研究所長,16年現職。13年よりバイオインダストリー協会運営会議委員,15年より政府のゲノム医療実現推進協議会構成員を務める。現在の研究はADCを含む新規バイオ医薬品の開発。
いま話題の記事
-
人工呼吸器の使いかた(2) 初期設定と人工呼吸器モード(大野博司)
連載 2010.11.08
-
忙しい研修医のためのAIツールを活用したタイパ・コスパ重視の文献検索・管理法
寄稿 2023.09.11
-
寄稿 2016.03.07
-
連載 2010.09.06
-
事例で学ぶくすりの落とし穴
[第7回] 薬物血中濃度モニタリングのタイミング連載 2021.01.25
最新の記事
-
医学界新聞プラス
[第5回]事例とエコー画像から病態を考えてみよう「腹部」
『フィジカルアセスメントに活かす 看護のためのはじめてのエコー』より連載 2024.04.12
-
医学界新聞プラス
[第3回]学会でのコミュニケーションを通して自分を売り込む!
『レジデントのためのビジネススキル・マナー――医師として成功の一歩を踏み出す仕事術55』より連載 2024.04.12
-
医学界新聞プラス
[第1回]心理社会的プログラムと精神障害リハビリテーションはどこが違うのでしょうか
『心理社会的プログラムガイドブック』より連載 2024.04.12
-
医学界新聞プラス
[第2回]小児Monteggia骨折
『クリニカル・クエスチョンで考える外傷整形外科ケーススタディ』より連載 2024.04.12
-
対談・座談会 2024.04.09
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。
