関節リウマチの診断・治療(高田和生)
連載
2011.10.10
もう膠原病は怖くない!
臨床医が知っておくべき膠原病診療のポイント
◆その5◆
関節リウマチの診断・治療
高田和生(東京医科歯科大学 医歯学融合教育支援センター 准教授)
(2944号よりつづく)
膠原病は希少疾患ですが,病態はさまざまな臓器におよび,多くの患者で鑑別疾患に挙がります。また,内科でありながらその症候は特殊で,多くは実際の診療を通してでなければ身につけにくいです。本連載では,膠原病を疑ったとき,膠原病患者を診るとき,臨床医が知っておくべきポイントを紹介し,膠原病専門診療施設での実習・研修でしか得られない学習機会を提供します。
| 【ケース】 36歳女性。半年ほど前から手・指関節痛が出現。リウマトイド因子陰性,X線検査で骨びらんなく,NSAIDsの服用のみで経過観察とされてきた。関節症状や倦怠感などもあり,現在就業困難。MRI検査を行ったところ,滑膜炎所見を認めた。 関節リウマチ(Rheumatoid Arthritis; RA)の診断は妥当か?初期治療はどのように行うか? |
RAの診療においては,次に記す4つの要素が主な原動力となり,この15年でパラダイムシフトが起こりました。
(1)関節破壊の進行が予想していたより早いと判明した,(2)発症後早期の炎症沈静化の重要性が認識された,(3)早期診断に役立つ検査(免疫血清検査/画像)が開発された,(4)有効性の高い治療法が開発された。
これらに触れながら,今日のRA診療を紹介します。
(!)発症4か月で,すでに40%の症例で骨破壊が見られる
骨破壊は時間を経てゆっくり進むため,安全性に懸念のある免疫抑制薬の早期使用はリスク・ベネフィットバランスが悪いと以前は理解されていました。しかし,単純X線でも発症1年後に15-30%が,MRIでは発症4か月後に45%もの患者が骨破壊を呈することがわかり(骨びらんの前駆病変とされる骨髄浮腫や,滑膜炎所見の頻度はさらに高い),リスク・ベネフィットバランスの再検討が必要になりました。
(!)発症後早期の炎症鎮静化達成は,長期にわたる治療反応性をも改善させる
発症後早期に適切な治療により炎症の鎮静化を図ることは,単に破壊進行期間を短縮するだけにとどまらず,長期にわたる治療反応性をも改善させ,これまでの治療戦略では極めてまれであったドラッグフリーでの長期的寛解維持を可能にする場合もあります。この「早期」とはRA発症後2年以内(window of opportunity)と言われています。
(!)RAの分類基準が2010年に改訂された
RAには確定診断はなく,臨床研究のために存在する分類基準を参考に臨床的に診断します。従来の分類基準[1987年米国リウマチ学会(ACR)作成]は平均発症8年後で疾患が確立し関節破壊も進行した患者データを基に,他の確立した関節炎疾患と区別すべく作成されたものでした。したがって,早期診断においては参考になりません。そこで,ACRおよび欧州リウマチ学会(EULAR)がRAの早期分類基準を作成し,2010年に発表しました(図1)。臨床現場では,この分類基準を参考に,早期診断が求められます。
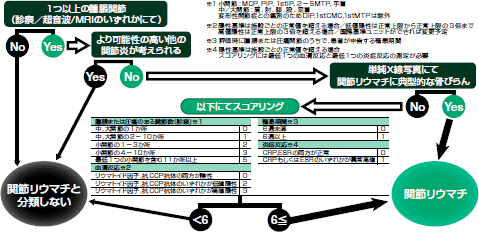 |
| 図1 米国リウマチ学会/欧州リウマチ学会による関節リウマチ分類基準 より早期での分類を目的に作られた基準のため,1987年ACR分類基準と比較し感度が高まり特異度が下がる。「より可能性の高い他の疾患が考えられる」場合はRAと分類できないとされており,この鑑別が重要。 |
(!)RAの治療目標はSDAI≦3.3
一般的に疾患の治療目標は,ADL/QOLが回復し,長期的障害が残らない水準の疾患活動性に設定されます。RAと同じ慢性疾患である糖尿病の治療目標が明確に示されているように,RAにおいても,ADL/QOLが回復し,骨破壊が進行して長期的ADL障害が残らない水準の疾患活動性であるべきで,次に記すACR/EULAR新寛解基準2011(臨床研究での使用が本来の目的)が参考になります。
(1)腫脹関節数,圧痛関節数,患者の疾患活動性全般評価[(Visual Analogue Scale; VAS)にて0-10cm],CRP(mg/dL)のすべてが1以下
(2)Simple Disease Activity Index(SDAI)[圧痛関節数(0-28)+腫脹関節数(0-28)+医師の疾患活動性全般評価(VASで0-10cm)+患者の疾患活動性全般評価(VASで0-10cm)+CRP(mg/dL)]≦3.3
((1)(2)のいずれかを満たす)
本基準の作成に際しては,実際の臨床試験データに当てはめ,骨破壊進行および中期的ADL障害の危険が最も小さい基準が選ばれました。しかし危険性はゼロではなく,また2年超の長期的予後との関係も未知であるため,本基準達成の場合でも,定期的にX線検査などで骨破壊の進行の有無の確認が必要です。また,治療の安全性も含めてリスク・ベネフィットバランスを考察し,場合によっては本基準より若干緩い基準(寛解ではなく低疾患活動性)を治療目標にすることもあります。
(!)治療は喘息治療と同じく,リリーバーとコントローラーの組み合わせ
同一患者における同一治療下でのRAの疾患活動度は,発症後まもなくはプラトーに達するまで上昇しますが,その後はほぼ一定水準を推移し,季節,感染症,ストレスなどにより若干変動します。一方妊娠中は6-7割で低下し,また産後はほぼ9割で上昇します。
RAの治療薬は,炎症の制御を速やかに達成するリリーバー(NSAIDs,低用量ステロイド経口,ステロイド関節内注射)と,長期的に炎症/自己免疫病態を制御するコントローラー(生物学的製剤も含む,図2)とに分類されます。基本的には寛解基準を目標に,コントローラーの投与量や組み合わせを1-3か月ごとに調整していきます。ただ,コントローラーの多くは作用発現に2-3か月ほどかかるため,初期治療導入時や増悪時でADL障害が強いときなどは,リリーバーも一時的に使用します。
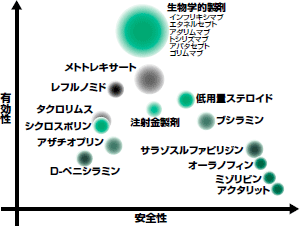 |
| 図2 RA治療におけるコントローラー薬剤の安全性と有効性(文献データおよび筆者の経験を踏まえて) |
なお低用量ステロイド経口療法にはコントローラーとしての作用もありますが,コントローラーの種類が増えた現在,骨粗鬆症などの蓄積的副作用もあり,長期的に続けられることはあまりありません。
(?)生物学的製剤は高額で危険なため,一部の患者にしか使われていない?
生物学的製剤の副作用には,投与部反応(注射の場合)や投与時反応(点滴の場合),結核を含めた重症感染症[生物学的製剤非使用RA患者の2倍,有害必要数(Number Needed to Harm ; NNH)は59],既存心不全の増悪,悪性腫瘍(懸念はあるがデータは一定しない)などがあります。また高額療養費制度を含む保険診療であっても高額(一般的な家計収入で計算した場合,年間40-50万円)になります。したがって,導入においては,治療による短期的および長期的ADL/QOLの改善とともに,これら安全性や費用の面を考慮します。現在日本に60-100万人いるといわれているRA患者のうち,14万人ほどに使用されています。
(?)寛解達成は生物学的製剤を使わなければ不可能である?
寛解達成のために必要なコントローラー(またはその組み合わせ)は,患者の疾患活動度により異なります。疾患活動度が低い場合はブシラミンなどの単剤で,疾患活動度が高い場合でも生物学的製剤を含まない複数の薬剤併用で寛解を達成できる場合も多くあります。
| 【診療のまとめ】 診察にて小関節7つに腫脹と圧痛を認め,抗CCP抗体陽性であり,新分類基準を満たすことから臨床的にRAと診断。コントローラーとしてブシラミンを選択,ADL低下もあるためリリーバーとしてプレドニゾロン5 mg/日も開始した。症状は速やかに改善したが,3か月後の判定で寛解に達しなかったため,メトトレキサートを追加した。さらに3か月後の判定で寛解となり,プレドニゾロン漸減を開始した。 |
(つづく)
いま話題の記事
-
人工呼吸器の使いかた(2) 初期設定と人工呼吸器モード(大野博司)
連載 2010.11.08
-
寄稿 2016.03.07
-
連載 2010.09.06
-
事例で学ぶくすりの落とし穴
[第7回] 薬物血中濃度モニタリングのタイミング連載 2021.01.25
-
連載 2016.07.04
最新の記事
-
医学界新聞プラス
[第1回]心理社会的プログラムと精神障害リハビリテーションはどこが違うのでしょうか
『心理社会的プログラムガイドブック』より連載 2024.04.12
-
医学界新聞プラス
[第2回]小児Monteggia骨折
『クリニカル・クエスチョンで考える外傷整形外科ケーススタディ』より連載 2024.04.12
-
医学界新聞プラス
[第5回]事例とエコー画像から病態を考えてみよう「腹部」
『フィジカルアセスメントに活かす 看護のためのはじめてのエコー』より連載 2024.04.12
-
医学界新聞プラス
[第3回]学会でのコミュニケーションを通して自分を売り込む!
『レジデントのためのビジネススキル・マナー――医師として成功の一歩を踏み出す仕事術55』より連載 2024.04.12
-
対談・座談会 2024.04.09
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。
