中間解析と早期終了の問題点 その5(植田真一郎)
連載
2010.12.06
論文解釈のピットフォール
【第21回】
中間解析と早期終了の問題点 その5
植田真一郎(琉球大学大学院教授・臨床薬理学)
(前回からつづく)
最近の新聞記事で,がんワクチン臨床試験の有害事象の取り扱いについて問題にしたものがありました。この試験に関する詳細な情報は持っていないので,その報道の是非を論じることはできません。しかし1つだけ言えるのは,未承認薬の臨床試験の実施に当たっては,重篤な有害事象の情報は参加した研究者間で,たとえ別のがんの試験においても,実施施設倫理委員会への報告などを通して正式に共有する必要がある,ということです。因果関係の有無は問われません。このことは,治験ではGCP(Good Clinical Practice;医薬品の臨床試験の実施に関する基準)により定められていますが,がんワクチンは未承認薬ですから,有害事象の取り扱いも同様に行ったほうが,より安全な試験の実施が可能だと思います。
日本では,承認を目的とした治験以外の臨床試験に関しては規制がなく,現時点では厚生労働省の「臨床研究に関する倫理指針」があるのみです。しかし,GCPも結局は試験参加患者の安全性を確保し,データの信頼性を担保しようとするものですから,本来はすべての臨床試験に適用できるはずなのです。ただ,すぐにover quality,overregulationをめざしてしまう日本では,「すべての臨床試験にGCPを適用してしまうと,本来の医師主導型研究が進まなくなる」「試験費用の高騰につながり,結局製薬会社の利益につながりやすい研究しか実施できず,社会に対しての有害なバイアスになる」などの問題も指摘されています。
またすべての臨床試験が承認申請をめざすわけではなく,前回取り上げたASCOT-BPLA試験のように,すでに治験を終えて承認された薬物を用いた治療法を比較する研究もあり,こちらにも同じ規制を適用させるのは考えものです。はじめに規制ありきではなく,研究ごとに被験者の安全性とデータの信頼性を担保するためにはどうすればよいかという現実的な視点が必要ですね。そして臨床試験では,主として被験者に対する試験自体の倫理性が議論されますが,社会に対する倫理性も考慮する必要があります。早期終了の倫理的な問題とはまさにそこなのです。
研究の過大評価は誰にどのような不利益をもたらすのか
前回も述べたように,早期終了で起こりやすい最も重要な問題は,結果の過大評価です。執筆者は,自分の論文について「治療法の効果を過大評価しているかもしれない」などとは絶対に書かないので,診療する側が気をつけて結果を読むしかありません。直接読むことができればまだいいのですが,これがガイドラインに掲載されたり,保険適応になったりすると,より多くの患者さんに影響します。
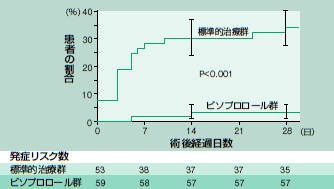
例えば,非心臓手術を受けるハイリスク患者において,β遮断薬が周術期の心事故の予防に有効かどうかは未だに議論があるところです。周術期のβ遮断薬は,1999年にわずか112人の患者を対象としたランダム化比較試験によって有効とされました1)。その後AHA/ACCのガイドラインにも掲載されていますが,この試験も早期終了したものです。結果(図1)は劇的で,β遮断薬非使用群では周術期心臓死が9件,非致死性心筋梗塞が9件発生しましたが,β遮断薬使用群では2件の周術期心臓死が発生しただけでした。
 |
|
図1 ビソプロロールと心血管イベント(文献1より改変)
標準的治療群とβ遮断薬ビソプロロール群の,一次エンドポイント(心臓死と非致死性心筋梗塞)のカプランマイヤー曲線。ビソプロロール群で,なんと91%のリスク減少が認められた。 |
たしかに,エンドポイントの発生は対照群で40%に近く,早期終了もあらかじめ決められた基準に則って行われています。しかし,やはりエンドポイント発生数が少ない場合は過大評価に陥る可能性が強いようで,その後のこの領域の臨床試験では有効性がはっきりしません2)。当時は臨床試験の登録制度がなかったので,出版バイアス(効果がないとした論文は出版されにくい)もあったのかもしれません。また,メタ解析も必ずしも信頼性は高くないですし,"バンドワゴンから飛び降りるのは難しい"バイアス(註)も出てきます。しかも掲載誌はprestigious journalです。逆に,「まだこの治療法に関しては確立されたエビデンスはありません」と言ってもなかなか信用されませんね。
臨床試験を実施して,科学的に妥当な結果を社会に提供することが臨床研究者の責務ですから,誤ったあるいは過大に評価された結果の提供は,社会に対して倫理的に問題があると言わざるを得ません。さらに薬物治療に関しては,"誰に""いつ""どのくらいの期間""どのような用量"を用いれば最善かという問題が常に発生します。早期終了により,あたかもこれらまでもが解決されたように誤解されることも問題です。
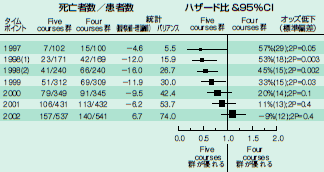
逆に,独立データ安全性モニタリング委員会の見識により早期終了を回避し,愚を冒すことなく正しい結果を得た場合もあります。前々回はCHARM試験についてお話ししましたが,急性骨髄性白血病(AML)の治療に関する比較試験でも,図2に示すように試験開始直後には劇的な死亡リスクの大きな減少が観察されていますが,観察を継続すると結局差異は見いだされませんでした3)。独立データ安全性モニタリング委員会は,初期の死亡リスクの劇的な減少は,医学的にimplausibleであることを主たる理由として試験を継続したわけですから,この見識により,AMLの患者さんは余計(かつ有害)な治療を受けなくて済んだわけです。
 |
|
図2 MRC AML試験中間解析における死亡リスクハザード比(文献3より改変)
中間解析における各治療群の死亡数とハザード比。初期の中間解析ではFive courses群で劇的な死亡リスクの減少が認められているものの,試験の継続により差は認められなくなった。 |
治療の安全性と有効性は慎重に,長期にわたり検討する
中間解析も含めて,主要評価項目を正しく評価することは,社会に対する倫理性という視点から最も重要な点ですが,早期終了は試験から得られるであろうさまざまな一次エンドポイント以外の情報にも影響します。前回,前々回で取り上げたJUPITER試験はCRP高値の健常者を対象とした試験であり,心筋梗塞の二次予防を目的とした患者が対象の試験とは異なります。つまり現時点では,薬物介入が必要だと考えられていない対象者における予防医学的な視点からの研究ですから,結果が公衆衛生に与える影響は大きく,治療の安全性と有効性を慎重に,より長期にわたって評価する必要があったのではないでしょうか。わずか1.9年間の観察期間は,この研究の目的を考えると適切ではありません。事実,主要評価項目ではありませんが,新規糖尿病の発症がロスバスタチン群で多いことが報告されています4)。
このように,エンドポイントとしては設定されていないものの長期間の薬物治療においては重要になる項目,特に副作用を評価する機会が早期終了により失われてしまう可能性は否定できません。もともと長期にわたる薬物療法を想定した試験なのに,「科学的に妥当な試験を行い,適切な情報を社会に提供する」ことになっていませんね。
ヘルシンキ宣言に謳われていたように,被験者の保護と有効とされた治療の現場への速やかな提供を目的とした中間解析と早期終了ですが,数回の連載でお話ししたように,現代では多くの問題点を抱えているようです。
(つづく)
註:効果があるとされた結果が支持され,ガイドラインにも掲載され,そこにある種のplausibilityが存在するとき,それに異を唱えるのは困難,というところで発生するバイアス。
参考文献
1)Poldermans D, et al. The effect of bisoprolol on perioperative mortality and myocardial infarction in high-risk patients undergoing vascular surgery. Dutch Echocardiographic Cardiac Risk Evaluation Applying Stress Echocardiography Study Group. N Engl J Med. 1999;341(24): 1789-94.
2)Juul AB, et al. Effect of perioperative beta blockade in patients with diabetes undergoing major non-cardiac surgery: randomised placebo controlled, blinded multicentre trial. BMJ. 2006; 332(7556): 1482.
3)Wheatley K, et al. Be skeptical about unexpected large apparent treatment effects: the case of an MRC AML12 randomization. Control Clin Trials. 2003; 24(1): 66-70.
4)Ridker PM, et al; JUPITER study group. Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein. N Engl J Med. 2008; 359(21): 2195-207.
いま話題の記事
-
忙しい研修医のためのAIツールを活用したタイパ・コスパ重視の文献検索・管理法
寄稿 2023.09.11
-
人工呼吸器の使いかた(2) 初期設定と人工呼吸器モード(大野博司)
連載 2010.11.08
-
連載 2010.09.06
-
事例で学ぶくすりの落とし穴
[第7回] 薬物血中濃度モニタリングのタイミング連載 2021.01.25
-
寄稿 2016.03.07
最新の記事
-
医学界新聞プラス
[第3回]人工骨頭術後ステム周囲骨折
『クリニカル・クエスチョンで考える外傷整形外科ケーススタディ』より連載 2024.04.19
-
医学界新聞プラス
[第2回]心理社会的プログラムを分類してみましょう
『心理社会的プログラムガイドブック』より連載 2024.04.19
-
医学界新聞プラス
[第1回]心理社会的プログラムと精神障害リハビリテーションはどこが違うのでしょうか
『心理社会的プログラムガイドブック』より連載 2024.04.12
-
医学界新聞プラス
[第2回]小児Monteggia骨折
『クリニカル・クエスチョンで考える外傷整形外科ケーススタディ』より連載 2024.04.12
-
医学界新聞プラス
[第5回]事例とエコー画像から病態を考えてみよう「腹部」
『フィジカルアセスメントに活かす 看護のためのはじめてのエコー』より連載 2024.04.12
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。
