非盲検試験で信頼性の高い結果を得るには(植田真一郎)
連載
2010.05.10
論文解釈のピットフォール
【第14回】
非盲検試験で信頼性の高い結果を得るには
植田真一郎(琉球大学大学院教授・臨床薬理学)
(前回からつづく)
ランダム化臨床試験は,本来内的妥当性の高い結果を提供できるはずですが,実に多くのバイアスや交絡因子が適切に処理されていない,あるいは確信犯的に除 去されないままです。したがって解釈に際しては,“ 騙されないように” 読む必要があります。本連載では,治療介入に関する臨床研究の論文を「読み解き,使う」上での重要なポイントを解説します。
前回は,臨床研究のなかには二重盲検が必須の“efficacy評価型”の臨床試験と,必ずしも二重盲検でなくてもよい,あるいは二重盲検の実施が不可能な“effectiveness 評価型”試験や研究があり,それぞれが患者へ治療を提供する,という目的において必要な研究であることをお話ししました。どちらに属すかはっきり分けられない試験もありますが,試験をデザインするときに大切なのは,efficacyとeffectivenessのどちらが目的なのか,何をアウトカムとして評価するのか,介入および対照となる治療は何か,その試験では盲検化が可能か,あるいは必要なのかを考察することだと思います。
また,非盲検であればどのような形でバイアスを除去すればよいのかを考える必要があります。日本の学会では,しばしばこのあたりが混乱している研究を散見します。よくあるのは,研究の背景から考えるとefficacyを評価する研究をすべきなのに,デザインは完全なeffectiveness評価型になっている研究です。また逆に,effectivenessを評価しようとしているのに,研究計画はどこかの治験の計画書のコピー&ペーストである場合もあります。
研究は,何を,何のために知りたいのかをはっきりさせてから計画すべきですが,残念ながら,日本には臨床研究を学ぶ確立されたカリキュラムがありません。新薬の治験手法は,薬効(efficacy)を厳密かつ安全に評価するための規制,試験デザインやデータ管理,統計解析などが医師よりもむしろ生物統計学者の関与により研究され,進歩してきました。そのため,診療の現場での疑問を解決するような,医師が積極的に主導すべきeffectiveness評価型研究に関しては,疫学研究以外に方法論も確立しているとは言えないし,研究を主導すべき臨床医に対し,この領域に関するトレーニングを提供できるところもあまりないのです(図)。琉球大学では,毎年春と夏に臨床研究に関するワークショップを開催して臨床研究ができる医師を育成しようとしています。興味のある方はご連絡ください(http://www.med.u-ryukyu.ac.jp/material/1270704952_16479.pdf)。
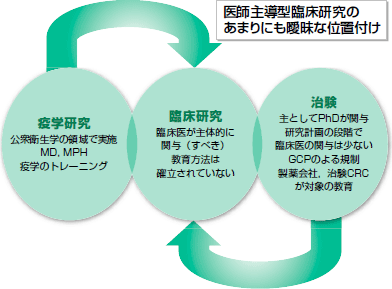 |
| 図 医師主導型臨床研究の曖昧な位置付け(原図=京大医学教育推進センター・森本剛講師) |
| 臨床上の疑問を解くためには,臨床医が主体的に関与すべき研究が多いが,その確立した教育プログラムはない。治験スタイルのガチガチプロトコルを無理やり当てはめて失敗したり,あまりにアバウトなプロトコルで失敗することも多い。資金が豊富ならプロトコル作成,データ管理にも準ずる“丸投げ”も行われている。 |
ストレプトマイシン研究におけるバイアスの除去
今回は,まず非盲検試験でもきちんと実施すれば信頼性の高い結果を得られるという例を挙げてみます。前回,盲検化は長い歴史を有することをお話ししましたが,ランダム化割り付けは1948年のMRC(Medical Research Council)ストレプトマイシン研究が最初です1)。この研究は,「ベッド上安静群」と「ストレプトマイシン投与+ベッド上安静群」の比較だったのですが,盲検化は行われませんでした。ストレプトマイシンの有効性を評価する初めての試験であり,プラセボを用いたほうがよかったかもしれません。しかし,研究者たちは対照群の患者にプラセボの注射を行うのは非倫理的と考え(これは一つの見識だと思います),オープン試験でありながら信頼性の高いデータを得るための研究計画を作成しました。
まず割り付け方法ですが,中央管理での封筒法を用いています。封筒法は原始的なランダム化割り付けの方法でご存じの方も多いと思いますが,うまくいかないことがあります。なぜなら,中央で管理しない限り,封筒を破棄して割り付け内容を見る,患者の状態に合わせて割り付けられた治療を拒否(どうしてもストレプトマイシンを投与したい場合,「ベッド上安静」と記載されていても「ストレプトマイシン」のカードを引くまで破棄!)するなど,選択バイアスが生じて交絡因子の混入が避けられないためです。
前回お話ししたように,このようにallocation concealment(割り付けの隠匿)が不可能になれば,結果に影響を及ぼします。例えば,日本で行われた九州脂質治療研究(KLIS)では,ランダム化割り付けは「研究に参加した医師によりneglectされた」と記載されているように,ルールが守られませんでした2)。そのため,コレステロール値は「医師の選択」によりプラバスタチン群で高値となり,対照群との比較が困難となりました。
同様に,カプトプリルとこれまでの降圧治療を比較したCAPPP研究(Captopril Prevention Project)では,封筒法によるランダム化の失敗でカプトプリル群の血圧が高く,脳卒中リスクなどに関する評価が困難だと思われます。封筒法,特に参加施設で開封する方法はできれば避けたほうがよいのですが,ストレプトマイシン研究では中央ランダム割り付け(中央の事務局で開封)によってこれを克服しています。割り付けは,各施設で6人分を乱数表により決定したのですが,この詳細も研究者には隠匿されていました。オープン試験でありながら,このような用心深い方法でallocation concealmentを確実にしたことにより,試験結果の信頼性を高めたと言えます。
適切なエンドポイントの評価法とは
もう一つ,ストレプトマイシン研究には重要な点があります。それは評価項目の客観性です。以前述べたことがありますが,オープン試験の方法の一つにPROBE(Prospective Randomised Open Blinded Endpoint)法があります3)。非盲検のランダム化比較試験のエンドポイント判定を,割り付け治療を知らされていない第三者が判定するというものですが,これまでの降圧薬と比較的新しい降圧薬を比較した臨床試験であるSTOP-2研究(Swedish Trial in Old Patients with Hypertension)において初めて使用されたと言われています。
しかし,このSTOP-2研究の45年前,このストレプトマイシン研究において,実はPROBE法は採用されていたのです。当時は,現在のように試験開始前に主要および副次的評価項目を宣言するということは行われていなかったようですが,抄録を読むと,ストレプトマイシン研究では,死亡および胸部X線の所見を主要な評価項目にしていたようです。
表にストレプトマイシン研究の結果を示します。結核での死亡率が高い時代背景を反映しているとも言えますが,前回お話ししたように,「死亡」は非盲検であることの影響を受けにくいのです。胸部X線の所見は割り付け治療を含む試験の内容をまったく知らない複数の専門医により読影されました。もちろん胸部X線の撮影は,決められた予定通りに行われています。X線での病状の把握は客観性に問題がないわけではありませんが,このような形をとることで問題を明らかに少なくしたわけです。
| 表 MRCストレプトマイシン研究の結果(文献1より改変) |
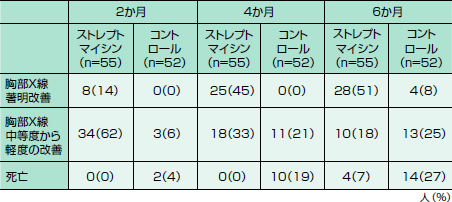 |
| ストレプトマイシン群では,安静のみの群と比較して死亡リスクが低く,また半数の患者で胸部X線所見の著明改善が見られた。 |
また,「死亡」という客観性の高い評価項目による結果と胸部X線という,言わばサロゲートマーカーの結果に,ストレプトマイシンの効果に関する一貫性があることも重要です。客観性に問題があっても,それが真のエンドポイント(死亡や心筋梗塞など)を予測できるものであれば評価する意義はありますし,次の試験やより短期間で薬効を評価したいときに役立ちます。
例えば,本連載にしばしば登場するJIKEI HEART STUDYでバルサルタンの効果があるとされた「狭心症での入院」はそれを示していません。ストレプトマイシン研究では,そのほかにも検査などの予定もあらかじめ定められていること,診療録のほかにCRF(Case report form;症例報告書)が作成され,今で言うモニタリングを実施していること,既にCRC(臨床研究コーディネーター)による試験支援実施が行われていることなど,試験の質を上げるためのさまざまな努力がなされています。このあたりの工夫をぜひ読み取るべきです。
(つづく)
参考文献
1) Medical Research Council. STREPTOMYCIN treatment of pulmonary tuberculosis. Br Med J. 1948 ; 2 (4582): 769-82.
2) The Kyushu Lipid Intervention Study Group. A coronary primary intervention study of Japanese men: study design, implementation and baseline data. J Atheroscler Thromb. 1996 ; 3 (2): 95-104.
3) Hansson L, et al. Prospective randomized open blinded end-point (PROBE) study. A novel design for intervention trials. Prospective Randomized Open Blinded End-Point. Blood Press. 1992 ; 1 (2): 113-9.
いま話題の記事
-
忙しい研修医のためのAIツールを活用したタイパ・コスパ重視の文献検索・管理法
寄稿 2023.09.11
-
人工呼吸器の使いかた(2) 初期設定と人工呼吸器モード(大野博司)
連載 2010.11.08
-
連載 2010.09.06
-
事例で学ぶくすりの落とし穴
[第7回] 薬物血中濃度モニタリングのタイミング連載 2021.01.25
-
寄稿 2016.03.07
最新の記事
-
医学界新聞プラス
[第3回]人工骨頭術後ステム周囲骨折
『クリニカル・クエスチョンで考える外傷整形外科ケーススタディ』より連載 2024.04.19
-
医学界新聞プラス
[第2回]心理社会的プログラムを分類してみましょう
『心理社会的プログラムガイドブック』より連載 2024.04.19
-
医学界新聞プラス
[第1回]心理社会的プログラムと精神障害リハビリテーションはどこが違うのでしょうか
『心理社会的プログラムガイドブック』より連載 2024.04.12
-
医学界新聞プラス
[第2回]小児Monteggia骨折
『クリニカル・クエスチョンで考える外傷整形外科ケーススタディ』より連載 2024.04.12
-
医学界新聞プラス
[第5回]事例とエコー画像から病態を考えてみよう「腹部」
『フィジカルアセスメントに活かす 看護のためのはじめてのエコー』より連載 2024.04.12
開く
医学書院IDの登録設定により、
更新通知をメールで受け取れます。
