連載
脳腫瘍
発生要因から遺伝子治療まで(9)
新しい放射線治療の臨床応用
高倉公明(東京女子医科大学付属脳神経センター所長)はじめに
脳腫瘍は悪性と良性脳腫瘍に2大別されているが,悪性脳腫瘍の治療には手術と放射線治療が基本的な治療法になっている。脳腫瘍の治療に放射線照射を導入したのは近代脳神経外科の基礎を確立した米国のHarvey Cushingで今世紀初頭のことであるから,脳腫瘍の放射線治療は80年以上の歴史を持っていることになる。
最近では各種の新しい放射線治療法が臨床に応用されるようになってきた。ガンマナイフ,リニアックを用いた定位的放射線治療,フォトン定位的放射線治療(Photon Radiosurgery System=PRS),重粒子線治療等が行なわれている。これらの放射線治療の考え方の根底には,腫瘍に対する局所放射線照射量を高めながら,周辺の正常脳に対する被曝量を最少にとどめる方法が求められている。
|
表1 日本におけるガンマナイフにより 治療が行なわれた症例数 (1995年12月末まで) | ||||||||
|
ガンマナイフは,約35年前にスウェーデンの脳神経外科医であったLeksellにより開発されたガンマ線局所放射線治療装置である。大きなヘルメット型の鉄製容器に201本のコバルト60小線源が埋めこまれており,ここから発生する微小な直径のガンマ線が一点に集中するように作られている。ガンマ線の焦点を病巣部に合わせることにより,局所には高エネルギーの放射線照射が行なわれるが,周辺の正常組織の被爆量は小さいため,局所的放射線治療が可能である。
当初スウェーデンでは,脳動静脈奇形や良性の聴神経腫瘍等の治療が始められた。その治療効果が次第に報告されるにつれて,1980年代以後,ガンマナイフは世界的に普及してきた。
1995年末までの世界の集計報告によると,ガンマナイフによる治療は全世界で約4万1000例行なわれており,その中で約3万例が脳腫瘍の治療である。日本では,1995年末までに約6600例の治療が行なわれており,その中の約2/3にあたる4400例が脳腫瘍の治療であった。治療の対象となった脳腫瘍の種類別の比率は表1に示した通りである。
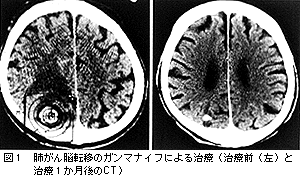
特に転移性脳腫瘍に対する治療効果は高く,多発性脳腫瘍でも4~5個の転移巣ならば,1日の治療で翌日退院することも可能である。腺がん,扁平上皮がんに対する治療効果も高く,直径3cm以下の転移巣ならば,約1か月でCT上消失し,その有効率も90%を越えている(図1)。
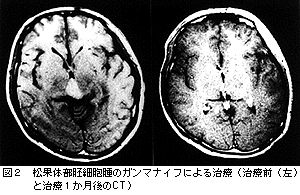
胚細胞腫も感受性が高く,一般的には照射後1か月ほどでCT上腫瘍像が消失する(図2)。一方,悪性神経膠腫(グリオーマ)は正常脳組織に広く浸潤する腫瘍であるから,局所的に治療効果があるガンマナイフの適応ではない。むしろ広範囲な照射に適したリニアックによる治療が適している。
しかし,再発した神経膠腫の再手術に代る治療手段として,また手術による摘出後の補助的局所療法として,さらに脳深部にあって手術による摘出が不可能ではあるが局所に限局している神経膠腫等に対しては,治療用具または方法の1つとしてガンマナイフによる治療は有効性を発揮する。
ガンマナイフは,聴神経腫瘍や髄膜腫,下垂体腺腫等の良性脳腫瘍の治療にも広く応用されている。しかし,基本的に手術が安全に行なえて全摘出可能な場合には,手術治療を選ぶべきである。
良性脳腫瘍に対するガンマナイフの治療効果は,悪性脳腫瘍と比較してきわめて緩徐に出現する。例えば,聴神経腫瘍や頭蓋底部の髄膜腫にガンマナイフによる照射を行なってから,CTやMRI上に認められる腫瘍縮小効果は,一般的に照射後2~3年を要する。下垂体腺腫で末端肥大症やクッシング病等の治療を行なった場合,血清中の成長ホルモンやACTHの値は照射後急速に低下することはなく,1年ほどかかって徐々に正常値に低下してくる。
脳腫瘍に対するガンマナイフ治療は,侵襲の少ない有効な治療法ではあるが,その適応は各腫瘍が持っている生物学的な特徴に応じた選択が必要である。
フォトン定位的放射線治療(PRS)
PRSは,米国のハーバード大とマサチューセッツ工科大で共同開発されたポータブル型の軟X線発生装置で,直径3mmの針の先端から軟X線が発射される。この装置は約10ボルトで稼働し,スイッチを入れるとX線が発射される。今日,アイソトープを用いた腫瘍の腔内照射が行なわれているが,PRSはこれに代わる用途を持っている。
軟X線は放射線のエネルギーが低いため,照射局所には高線量の放射線照射が可能であるが,中心から離れるとエネルギーは急速に低下するため,周辺組織への照射量も少なく,医療に従事する医師や看護婦等が放射線を被曝する危険の少ない安全な治療機器である。
PRSは手術で脳腫瘍を切除した際,残存する腫瘍に対して術中照射として使用する方法と,脳深部の腫瘍等に対して定位的生検を行なう際に,組織診断確認後に生検針と代えて局所放射線治療を行なう2通りの治療法がある。照射計画は,術前にコンピュータを用いて線量分布と線量をあらかじめ測定,決定しておく。照射線量は,腫瘍の周辺線量で定める。腫瘍の直径によって照射時間が異なってくるが,直径1cm程度の小さい腫瘍では数分,直径が3cm程度では数十分間の照射が必要になる。本法を用いて治療した症例を図3に示した。
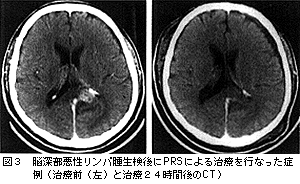
本例は視床部に近い腫瘍で,手術による摘出では重大な神経症候が発生する部位に存在した。生検で悪性リンパ腫と診断されたので,その際に局所に7分間,周辺線量10GyのPRSによる治療を行なった。悪性リンパ腫は放射線感受性が高い腫瘍であるが,本例では24時間後のCTでは腫瘍がすでに消失していた。
このように,PRSは局所的には有用な治療法である。転移性脳腫瘍はガンマナイフによる治療が一般的治療法だが,手術で摘出を行ない,その際に残存腫瘍にPRS治療を行なう方法は有効である。この方法で治療した肺がん脳転移の例では,治療1年後に局所の再発は認められなかった。
重粒子線治療
重粒子線によるがんの治療は,科学技術庁放射線総合医学研究所のシンクロトロンによって1994年より開始されている。頭頸部がん,肺がん等,臓器別に研究班が構成されており,中枢神経系腫瘍の研究班として,脳腫瘍の治療体制が組織されている。脳の深部に存在する腫瘍に対しても,放射線エネルギーを局所で最高に設定できる点は本治療法の大きな長所である。
現在,膠芽腫,悪性星細胞腫,頭蓋底部腫瘍等に対する治療が,炭素原子核による照射によって行なわれている。治療効果については,今後数年間の長期治療成績を比較しなければ結論することができないが,頭蓋底部の脊索腫のような広範囲に拡がる腫瘍に対しては,ガンマナイフによる治療能力の限界を越えるので,重粒子線治療の有用性が期待されている。
おわりに
今日では,上述したように悪性脳腫瘍の治療にさまざまな放射線治療が行なわれている。それぞれの治療法は利点と欠点があり,基本的にはそれぞれの病態に応じて,患者の生活の質(QOL)を向上するために最適の治療法を選択する必要がある。いずれの放射線治療装置も,治療のための道具の1つであると考えるのが正しいと思っている。
悪性脳腫瘍の治療には,手術,放射線治療,化学療法,BRMを用いた治療法等さまざまな治療手段があり,これまでにもそれぞれの有効性が記述,報告されてきた。治療にあたっては患者の予後を考えて,幸せな社会生活が永く続くことのみを願って,総合的観点から治療法を選択し,また種々の治療法を組み合わせて治療を行なうことがきわめて重要であることを強調しておきたい。